题目内容
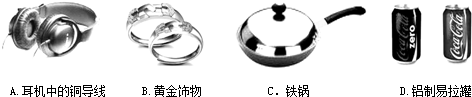
8.如图所示是生活中常见的金属物质.(1)如图所示生活用品中,主要利用金属导热性的是C(填字母).
(2)铝具有很好的抗腐蚀性,原因是4Al+3O2 =2Al2O3 (用化学方程式表示).
(3)某化学小组用铁丝、铜丝、银丝、稀硫酸和硫酸铜溶液,验证铁、铜、银的金属活动性顺序,实验结束后同学们欲对该实验的废液进行探究,他们先看到废液呈蓝色现象,认为废液中一定含有硫酸铜;还认为一定含有硫酸亚铁,依据是Fe+H2SO4=FeSO4+H2↑(或Fe+CuSO4=FeSO4+Cu)(用化学方程式回答).
分析 (1)金属具有良好的导电性、导热性、延展性;
(2)铝在空气中能与氧气反应形成致密的氧化物薄膜,铁锈的主要成分是氧化铁,氧化铁能和稀盐酸反应生成氯化铁和水;
(3)硫酸铜溶液是蓝色的,铁能和硫酸铜反应生成硫酸亚铁和铜.
解答 解:(1)金属具有良好的导热性,可以用来制作炊具.故填:C.
(2)铝在空气中能与氧气反应形成致密的氧化物薄膜,保护内部的铝不会进一步被腐蚀,故反应的化学方程式为:4Al+3O2 =2Al2O3 ;
(3)硫酸铜溶液是蓝色的,如果废液显蓝色,说明溶液中含有硫酸铜;铁和稀硫酸反应产生硫酸亚铁和氢气,和硫酸铜反应产生硫酸亚铁和铜;故填:废液呈蓝色;Fe+H2SO4=FeSO4+H2↑(或Fe+CuSO4=FeSO4+Cu).
点评 本题主要考查物质的性质和化学方程式的书写等方面的知识,充分认识反应进行的程度来分析金属与盐的置换反应发生的情况金属有剩余还是盐有剩余即可准确解答该题.

练习册系列答案
 优百分课时互动系列答案
优百分课时互动系列答案
相关题目
17. 如图是稀HCl和NaOH溶液反应的pH变化曲线,以下说法正确的是( )
如图是稀HCl和NaOH溶液反应的pH变化曲线,以下说法正确的是( )
 如图是稀HCl和NaOH溶液反应的pH变化曲线,以下说法正确的是( )
如图是稀HCl和NaOH溶液反应的pH变化曲线,以下说法正确的是( )| A. | 该反应是稀HCl滴入NaOH溶液中 | |
| B. | ag是指加入氢氧化钠固体质量 | |
| C. | B点溶液的溶质为NaOH和NaCl | |
| D. | 检验A点溶液的酸碱性可用无色酚酞溶液 |
19.物质的性质决定用途.下列对应关系成立的是( )
| A. | 石墨有滑腻感,可用作电极 | B. | 干冰升华吸热,可用作食品保鲜剂 | ||
| C. | 焦炭有还原性,可用作吸附剂 | D. | 金刚石无色透明,可用于切割玻璃 |
17.如图为某家长带小孩在下水道井盖小孔上点燃鞭炮发生爆炸的画面.现要探究某下水道的可燃性气体成分:

[猜想](I)含可燃性气体CO;
(Ⅱ)含可燃性气体CH4;
(Ⅲ)含可燃性气体CO和CH4.
[收集气体]用大的可乐塑料瓶装满水,打开瓶盖用绳子吊入下水道中,用铁钩将矿泉水瓶倒转,使瓶内水倒出,并将瓶口向下提到井口迅速盖好瓶备用.
[进行实验]
[作出判断]根据上述实验现象,甲同学认为猜想Ⅲ正确;而乙同学认为甲的判断不严谨.因为猜想也有相同的现象.如需进一步确认还应检验CO存在,其方法是将气体通过炽热的氧化铜粉末,看粉末是否变红
[拓展]若需要工人进入下水道清理淤泥,打开下水道井盖后应首先进行的操作是通风.

[猜想](I)含可燃性气体CO;
(Ⅱ)含可燃性气体CH4;
(Ⅲ)含可燃性气体CO和CH4.
[收集气体]用大的可乐塑料瓶装满水,打开瓶盖用绳子吊入下水道中,用铁钩将矿泉水瓶倒转,使瓶内水倒出,并将瓶口向下提到井口迅速盖好瓶备用.
[进行实验]
| 步骤 | 实验搡作 | 实验现象 | 结论 |
| (1) | 导出瓶中气体,通过装有氢氧化钠溶液的洗气瓶. | 无明显现象 | 目的是除CO2等酸性气体. |
| (2) | 再通过装有浓硫酸的洗气瓶. | 无明显现象 | 目的是除去水份,使气体干燥. |
| (3) | 将步骤(2)的气体导出点燃; ①在火焰上方罩一个干而冷的小烧杯 ② . | 无水硫酸铜 变蓝?; ? | ?证明有H2O生成; ?证明有CO2生成. |
[拓展]若需要工人进入下水道清理淤泥,打开下水道井盖后应首先进行的操作是通风.
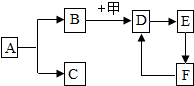 如图中的物质均是初中化学常见物质,其中A是常见的无色液体,F是大理石的主要成分,甲是生活里常用的燃料.根据它们之间的转化关系(有些反应条件、反应物、生成物已省略).回答下列问题:
如图中的物质均是初中化学常见物质,其中A是常见的无色液体,F是大理石的主要成分,甲是生活里常用的燃料.根据它们之间的转化关系(有些反应条件、反应物、生成物已省略).回答下列问题: