题目内容
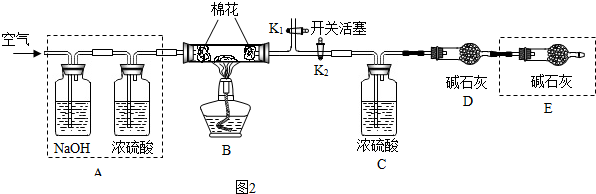
实验室通常采用如图装置制取少量干燥氢气,请根据要求回答: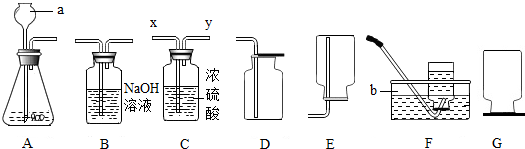
(1)仪器a的名称 ,仪器b的名称 .
(2)实验室使用稀盐酸和金属锌制取氢气,反应的化学方程式为 ;这种方法制得的氢气往往含有少量氯化氢气体和水蒸气两种杂质,这是因为盐酸具有 性,可以先通过 装置(填装置序号)除去氯化氢气体,然后通过C装置除去水蒸气,原理是装置中的浓硫酸具有 性,气体从C装置 处进入(填x或y).
(3)实验中可采用 装置收集干燥氢气.

(1)仪器a的名称
(2)实验室使用稀盐酸和金属锌制取氢气,反应的化学方程式为
(3)实验中可采用
考点:氢气的制取和检验,气体的净化(除杂),书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)认识常见仪器;
(2)锌与盐酸反应生成氯化锌和氢气;根据盐酸的挥发性和浓硫酸的吸水性来分析;
(3)根据氢气的性质以及不同收集方法的特点来分析.
(2)锌与盐酸反应生成氯化锌和氢气;根据盐酸的挥发性和浓硫酸的吸水性来分析;
(3)根据氢气的性质以及不同收集方法的特点来分析.
解答:解:(1)a是长颈漏斗,b是水槽;
(2)锌与盐酸反应生成氯化锌和氢气,化学方程式为:Zn+2HCl=ZnCl2+H2↑,盐酸具有挥发性,导致制取的氢气中混有氯化氢气体,可以利用氢氧化钠溶液来反应掉氯化氢气体,浓硫酸具有吸水性,可以除去氢气中混有的水蒸气,注意长进短出;
(3)排水法收集的氢气比较纯净,向下排空气法收集到的氢气比较干燥.
故答案为:(1)长颈漏斗;水槽;
(2)Zn+2HCl=ZnCl2+H2↑;挥发;B;吸水;x;
(3)E.
(2)锌与盐酸反应生成氯化锌和氢气,化学方程式为:Zn+2HCl=ZnCl2+H2↑,盐酸具有挥发性,导致制取的氢气中混有氯化氢气体,可以利用氢氧化钠溶液来反应掉氯化氢气体,浓硫酸具有吸水性,可以除去氢气中混有的水蒸气,注意长进短出;
(3)排水法收集的氢气比较纯净,向下排空气法收集到的氢气比较干燥.
故答案为:(1)长颈漏斗;水槽;
(2)Zn+2HCl=ZnCl2+H2↑;挥发;B;吸水;x;
(3)E.
点评:合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
物质的性质决定其用途.下列因果关系不成立的是( )
| A、洗洁精具有乳化功能,用于去除油污 |
| B、稀硫酸能与金属反应,用于去除铁锈 |
| C、钨的熔点高且能导电,用于制作白炽灯丝 |
| D、一氧化碳有还原性,工业上用来冶炼金属 |