题目内容
14.如图1是某同学完成《一定质量分数的氯化钠溶液的配制》中“配制50g质量分数为6%的氯化钠溶液”的全过程.
(1)图中的错误有:
①药品瓶盖正放在了桌面上,②砝码和药品位置颠倒;
(2)若所配制的盐水中NaCl的质量分数小于6%,则可能造成误差的原因有C;
A.量取水时俯视读数 B.玻璃棒使用前洗净擦干
C.使用的烧杯内壁有水珠 D.配置好的溶液转移时洒出一部分
(3)配制溶液还可以用浓溶液稀释得到,用浓度20%的氯化钠溶液配置50g质量分数为6%的氯化钠溶液,需要加水的体积是35mL;
(4)化学上还可以通过反应获得氯化钠溶液,向稀盐酸中逐滴滴加氢氧化钠溶液,pH变化如图2.试回答:
a点溶液中含有的离子有Na+、H+、Cl-.
分析 (1)取用固体药品时,瓶塞应倒放;托盘天平的使用要遵循“左物右码”的原则;据此进行分析解答.
(2)所配制溶液的质量分数小于所要配制的5%,由此可判断所配制的溶液中溶质氯化钠质量偏小或溶剂水的量偏大导致的结果,因此,在分析造成误差的原因时,应围绕这样两个原因分析可能造成误差的操作.
(3)根据溶液稀释过程中溶质的质量不变来分析;
(4)根据a点溶液的pH来分析.
解答 解:(1)①取用固体药品时,为防止污染药品,瓶塞应倒放,图中瓶塞没有倒放.
②托盘天平的使用要遵循“左物右码”的原则,图中砝码与氯化钠的位置放反了;
故填:①药品瓶盖正放在了桌面上; ②砝码和药品位置颠倒;
(2)A.量取水时俯视造成量取水的实际体积偏小,使所得溶液中水量偏少,配制的溶液的浓度偏大;
B.玻璃棒使用前洗净擦干,对实验结果无影响;
C.若烧杯内有水,造成水的量偏多,配制的溶液的浓度偏小;
D.配置好的溶液转移时洒出一部分,对溶液的浓度没有影响.
故选C;
(3)设需要加入水的质量为x,则
(50g-x)×20%=50g×6%
x=35g
水的体积为:35g÷1g/mL=35mL
故填:35mL;
(4)氢氧化钠与盐酸反应生成氯化钠和水,a点溶液的pH<7,显酸性,溶液中还存在HCl,故填:Na+、H+、Cl-.
点评 本题考查了溶液的配制,完成此题,可以依据已有的知识进行,要求同学们熟练掌握溶液配制的步骤和所需要的仪器,以便灵活应用.

练习册系列答案
 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案
相关题目
5.NH4H2PO4中氮元素的化合价为( )
| A. | -3 | B. | -1 | C. | +1 | D. | +3 |
19.下列说法正确的是( )
| A. | K2MnO4、KMnO4、MnO2三者中Mn元素的化合价逐渐升高 | |
| B. | HCl、NaCl、Na2CO3溶液的pH逐渐变大 | |
| C. | NH4NO3、NaCl、CaO三者溶于水后,所得溶液的温度逐渐降低 | |
| D. | 将Zn、Fe两金属片分别放入CuSO4溶液中可以证明三种金属的活动性顺序为Zn>Fe>Cu |

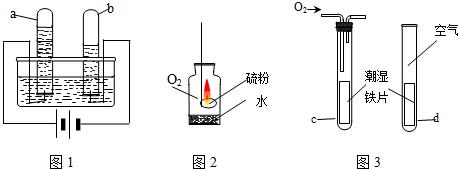
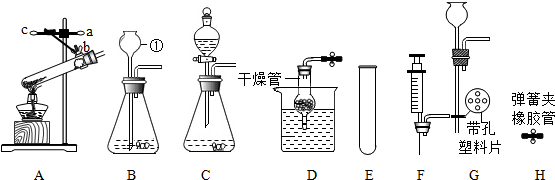
 如图是a、b、c三种物质溶解度曲线,a与c溶解度曲线相交于P点.据图回答:
如图是a、b、c三种物质溶解度曲线,a与c溶解度曲线相交于P点.据图回答: