题目内容
32.5克锌粒与280克稀硫酸恰好完全反应.试求:(相对原子质量 H:1 S:32 Zn:65 O:16)
(1)稀硫酸中溶质的质量分数.
(2)生成物溶液中溶质的质量分数.
(1)稀硫酸中溶质的质量分数.
(2)生成物溶液中溶质的质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:溶质质量分数与化学方程式相结合的计算
分析:锌和稀硫酸反应生成硫酸锌和氢气;
根据锌的质量可以计算硫酸、硫酸锌、氢气的质量,进一步可以计算稀硫酸中溶质的质量分数和生成物溶液中溶质的质量分数.
根据锌的质量可以计算硫酸、硫酸锌、氢气的质量,进一步可以计算稀硫酸中溶质的质量分数和生成物溶液中溶质的质量分数.
解答:解:(1)设硫酸的质量为x,生成硫酸锌的质量为y,生成氢气的质量为z,
Zn+H2SO4═ZnSO4+H2↑,
65 98 161 2
32.5g x y z
=
=
=
,
x=49g,y=80.5g,z=1g,
稀硫酸中溶质的质量分数为:
×100%=17.5%,
答:稀硫酸中溶质的质量分数为17.5%.
(2)生成物溶液中溶质的质量分数为:
×100%=25.8%,
答:生成物溶液中溶质的质量分数为25.8%.
Zn+H2SO4═ZnSO4+H2↑,
65 98 161 2
32.5g x y z
| 65 |
| 32.5g |
| 98 |
| x |
| 161 |
| y |
| 2 |
| z |
x=49g,y=80.5g,z=1g,
稀硫酸中溶质的质量分数为:
| 49g |
| 280g |
答:稀硫酸中溶质的质量分数为17.5%.
(2)生成物溶液中溶质的质量分数为:
| 80.5g |
| 32.5g+280g-1g |
答:生成物溶液中溶质的质量分数为25.8%.
点评:本题主要考查学生运用假设法和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
在氯酸钾里加入了少量的高锰酸钾后,加热时制取氧气的速率大大加快,其主要原因是( )
| A、高锰酸钾比氯酸钾容易分解 |
| B、高锰酸钾起了催化作用 |
| C、高锰酸钾受热分解,使产生的氧气增多 |
| D、高锰酸钾受热分解生成的二氧化锰成为氯酸钾受热分解时的催化剂 |
固体氢氧化钠和氧化钙的混合物叫做碱石灰,常用作干燥剂.下列气体不能用碱石灰干燥的是( )
| A、CO |
| B、H2 |
| C、HCl |
| D、O2 |
下列属于化学变化的是( )
| A、电灯通电发光 | B、轮胎爆炸 |
| C、米酿成醋 | D、海水晒盐 |
这种饮用天然水呈( )
| A、酸性 | B、碱性 |
| C、中性 | D、无法确定 |
芦山大地震导致灾区部分水源严重污染,为保障当地群众饮水安全,需要消毒杀菌.有关卫生防疫部门使用的消毒剂主要有:优氯净(C3O3N3Cl2Na)、二氧化氯(C1O2)、“84”消毒液(有效成分为NaClO).下列有关说法错误的是( )
| A、消毒杀菌的过程是化学变化 |
| B、C3O3N3Cl2Na的相对分子质量为232.5 |
| C、C3O3N3Cl2Na中C、N、O元素的质量比为6:7:8 |
| D、三种消毒剂中C3O3N3Cl2Na属于有机化合物 |
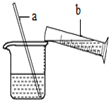 如图是稀释浓硫酸实验的示意图.
如图是稀释浓硫酸实验的示意图.