题目内容
3.在鱼缸里加入“鱼浮灵”,能增加水中的含氧量.“鱼浮灵”的化学名称是过氧碳酸钠(俗称固体双氧水,化学式2Na2CO3•3H2O2),它溶于水后能生成Na2CO3和H2O2.一天,小科用“鱼浮灵”进行了甲、乙两图所示的实验.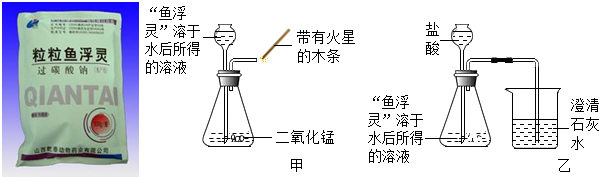
(1)在甲图所示的实验中,小科观察到锥形瓶内有气泡放出,带火星的木条复燃.请写出该锥形瓶中发生反应的化学方程式:2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,该反应属于分解反应(填化学反应的基本类型).
(2)在乙图所示的实验中,观察到锥形瓶内有气泡放出,烧杯中澄清石灰水变浑浊.该实验中,小科运用了Na2CO3与盐酸的反应原理.
分析 (1)由题目的信息可知:向试管中加入少量MnO2粉末,产生大量气泡,将带火星木条伸入试管,木条复燃,说明有O2生成;据此写出反应的方程式并判断反应类型;
(2)根据碳酸钠和盐酸反应生成氯化钠和水和二氧化碳,因此二氧化碳能使澄清的石灰水变浑浊分析.
解答 解:(1)由题目的信息可知:向试管中加入少量MnO2粉末,产生大量气泡.将带火星木条伸入试管,木条复燃,说明有O2生成;因此该反应是过氧化氢在二氧化锰的作用下分解产生水和氧气,该反应是一种物质生成两种物质的分解反应;故填:2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;分解;
(2)碳酸钠和盐酸反应生成氯化钠和水和二氧化碳,因此二氧化碳能使澄清的石灰水变浑浊;故填:变浑浊.
点评 本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
2.如图所示变化过程中发生物理变化的是( )
| A. |  蜡烛燃烧 | B. |  动植物的呼吸 | ||
| C. |  松花江水面结冰 | D. |  铜在潮湿的空气中生成铜绿 |
14.某化学兴趣小组的同学往氢氧化钠溶液中滴加稀盐酸时,没有看到明显现象.
【提出问题】氢氧化钠与盐酸是否发生了化学反应?
【查阅资料】酸与碱发生中和反应会放出热量.
【实验设计】甲、乙、丙三位同学分别设计了如下实验方案,请你帮他们完成实验报告.
【评价反思】你认为实验设计方案不合理的同学是乙,理由是氢氧化钠固体溶于水也会放出热量.
【提出问题】氢氧化钠与盐酸是否发生了化学反应?
【查阅资料】酸与碱发生中和反应会放出热量.
【实验设计】甲、乙、丙三位同学分别设计了如下实验方案,请你帮他们完成实验报告.
| 同学 | 实验操作 | 现象 | 结论 |
| 甲 |  | 溶液由红色变成无色 | 氢氧化钠与盐酸发生了化学反应,反应的化学方程式为HCl+NaOH=NaCl+H2O |
| 乙 | 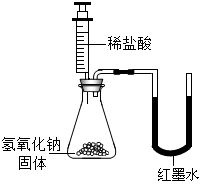 | U形玻璃管中左边的红墨水液面下降(所加稀盐酸的体积忽略不计) | 氢氧化钠与盐酸发生了化学反应 |
| 丙 | 用pH试纸测定氢氧化钠溶液的pH;向其中滴加足量的稀盐酸后,再测定溶液的pH | 最后溶液的pH≤7(填“≥7”“≤7”或“不变”) | 氢氧化钠与盐酸发生了化学反应 |
11.下列说法,正确的是( )
| A. | 水是取之不尽、用之不竭的资源 | |
| B. | 自然界的水主要用于人们的日常饮用 | |
| C. | 凡是无色透明的水都是能饮用的 | |
| D. | 工农业用水也主要是淡水 |
15.分类是学习和研究物质及其变化的一种常用方法.分类要有一定的标准,如果按照物质的组成对赤铁矿、纯碱、氧气、烧碱、水、硫酸六种物质进行分类,则图中虚线框内的①、②、③、④、⑤、⑥依次为( )
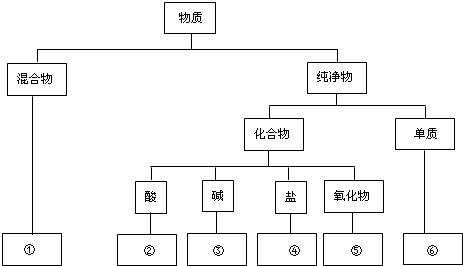

| A. | 赤铁矿、硫酸、纯碱、烧碱、水、氧气 | B. | 水、硫酸、烧碱、纯碱、赤铁矿、氧气 | ||
| C. | 赤铁矿、硫酸、烧碱、纯碱、水、氧气 | D. | 水、硫酸、纯碱、烧碱、赤铁矿、氧气 |
12.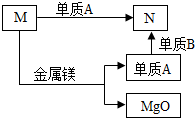 纯净物M、N之间存在着如图所示的转化关系,且反应物和生成物均表示在图示中.单质A和单质B分别由A、B元素组成.据此,有以下的说法:①M是氧化物;②M、N中只有N含有A元素;③N不是氧化物;④M与镁的反应是置换反应;在这些说法中正确的有( )
纯净物M、N之间存在着如图所示的转化关系,且反应物和生成物均表示在图示中.单质A和单质B分别由A、B元素组成.据此,有以下的说法:①M是氧化物;②M、N中只有N含有A元素;③N不是氧化物;④M与镁的反应是置换反应;在这些说法中正确的有( )
 纯净物M、N之间存在着如图所示的转化关系,且反应物和生成物均表示在图示中.单质A和单质B分别由A、B元素组成.据此,有以下的说法:①M是氧化物;②M、N中只有N含有A元素;③N不是氧化物;④M与镁的反应是置换反应;在这些说法中正确的有( )
纯净物M、N之间存在着如图所示的转化关系,且反应物和生成物均表示在图示中.单质A和单质B分别由A、B元素组成.据此,有以下的说法:①M是氧化物;②M、N中只有N含有A元素;③N不是氧化物;④M与镁的反应是置换反应;在这些说法中正确的有( )| A. | ①② | B. | ②④ | C. | ①④ | D. | 只有④正确 |
13. 铅中毒会造成儿童多动症,影响智力,铅的相对原子质量是207,与铁相差很大.那么铅与铁的金属活动性谁更强些?某兴趣小组进行了探究:
铅中毒会造成儿童多动症,影响智力,铅的相对原子质量是207,与铁相差很大.那么铅与铁的金属活动性谁更强些?某兴趣小组进行了探究:
实验设计:相同温度下,取大小相同的两种金属薄片,用砂纸将表面擦光亮,分别投入等体积、等浓度且足量的稀盐酸中反应,观察现象.
请分析回答下列问题:
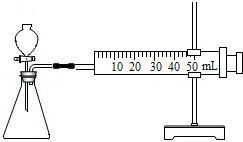
(1)连接仪器组装成如右图所示.某学生用抽拉法检查该装置的气密性,发现被拉出的针筒活塞一段时间后又回到原来的位置,你认为该装置是否漏气?不漏气.
(2)根据下表中的现象填写结论.
请写出铁与盐酸反应的化学方程式:Fe+2HCl=FeCl2+H2↑
(3)除了比较与酸反应产生气体速度的快慢,你还有其他化学方法可以比较金属活动性的强弱吗?请举出一种方法(写出原理即可)Pb+FeCl2=Fe+PbCl2.
 铅中毒会造成儿童多动症,影响智力,铅的相对原子质量是207,与铁相差很大.那么铅与铁的金属活动性谁更强些?某兴趣小组进行了探究:
铅中毒会造成儿童多动症,影响智力,铅的相对原子质量是207,与铁相差很大.那么铅与铁的金属活动性谁更强些?某兴趣小组进行了探究:实验设计:相同温度下,取大小相同的两种金属薄片,用砂纸将表面擦光亮,分别投入等体积、等浓度且足量的稀盐酸中反应,观察现象.
请分析回答下列问题:
(1)连接仪器组装成如右图所示.某学生用抽拉法检查该装置的气密性,发现被拉出的针筒活塞一段时间后又回到原来的位置,你认为该装置是否漏气?不漏气.
(2)根据下表中的现象填写结论.
| 金属 | 铁 | 铅 |
| 与盐酸反应现象 | 放出气泡速度缓慢 | 放出气泡速度较快 |
| 结论 | 铅比铁的金属活动性强 | |
(3)除了比较与酸反应产生气体速度的快慢,你还有其他化学方法可以比较金属活动性的强弱吗?请举出一种方法(写出原理即可)Pb+FeCl2=Fe+PbCl2.