题目内容
5.质量相等的锌、铝、铁分别与足量稀盐酸反应,产生氢气的质量( )| A. | 锌最多,铁最少 | B. | 铝最多,锌最少 | C. | 铁最多,铝最少 | D. | 三者一样多 |
分析 根据金属元素的相对原子质量和它们与稀盐酸反应的化学方程式,计算出1g这些金属分别与足量稀盐酸反应生成氢气的质量,再进行比较即可.
解答 解:根据化学方程式:2Al+6HCl═2AlCl3+3H2↑;Zn+2HCl═ZnCl2+H2↑Fe+2HCl═FeCl2+H2↑;
可以看出:Al的相对原子质量为27,54g铝可反应生成6g氢气,所以1g铝生成氢气$\frac{1}{9}$g,
Zn的相对原子质量为65,65g锌可反应生成2g氢气,即1g锌生成$\frac{1}{32.5}$克氢气.
铁的相对原子质量56,56g铁可反应生成2g氢气,即1g铁生成$\frac{1}{28}$g氢气.
所以$\frac{1}{9}>\frac{1}{28}>\frac{1}{32.5}$,铝生成的氢气最多,锌生成的氢气最少.
故选:B.
点评 本题主要考查学生运用化学方程式综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目
15.如图所示的下列实验装置或操作中,不正确的是( )
| A. |  检查装置气密性 | B. |  点燃酒精灯 | ||
| C. | 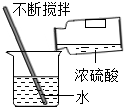 稀释浓硫酸 | D. |  测定空气里氧气含量 |
16.我们熟悉的下列物质中属于纯净物的是( )
| A. | 牛奶 | B. | 食醋 | C. | 空气 | D. | 蒸馏水 |
4. 2015年2月,中德科学家成功合成了具有优异的电化学性能的钒的氧化物(V6O13).钒元素的相关信息如图.下列有关钒的说法错误的是( )
2015年2月,中德科学家成功合成了具有优异的电化学性能的钒的氧化物(V6O13).钒元素的相关信息如图.下列有关钒的说法错误的是( )
 2015年2月,中德科学家成功合成了具有优异的电化学性能的钒的氧化物(V6O13).钒元素的相关信息如图.下列有关钒的说法错误的是( )
2015年2月,中德科学家成功合成了具有优异的电化学性能的钒的氧化物(V6O13).钒元素的相关信息如图.下列有关钒的说法错误的是( )| A. | 原子的核电荷数是23 | B. | 元素符号是V | ||
| C. | 相对原子质量为50.94g | D. | 属于金属元素 |
5.下列实验现象的描述正确的是( )
| A. | 木炭在空气中燃烧,产生蓝色火焰 | |
| B. | 稀硫酸中滴加石蕊溶液,溶液变红 | |
| C. | 镁条在氧气中燃烧,生成黑色固体 | |
| D. | 氢氧化钠溶液中滴加硫酸铜,产生白色沉淀 |