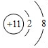题目内容
下图是初中化学常见的四个实验,请回答下列问题。

(1)A实验验证铁生锈的条件是铁与 共同作用;
(2)B实验中没有出现预期的实验现象,可能的原因是 ;
(3)C实验中导致实验结果偏小的原因之一是 ;
(4)D实验中烧杯中热水的作用是 。
(1)氧气和水(或O2和H2O)
(2)氧气浓度不够(或铁丝事先没打磨等其他合理即给分)
(3)红磷量不足(或装置气密性不好等其他合理即给分)
(4)提高铜片上白磷的温度并使水中白磷隔绝氧气
【解析】
试题分析:(1)铁生锈的实质是铁与空气中的氧气或水分共同作用的结果。
(2)没有符合燃烧条件,如温度没有达到铁丝的着火点,或氧气浓度低,或铁丝表面有漆等;
(3)测得氧气含量低于五分之一的原因:红磷量不足,或装置漏气,或未冷却至室温就打开了弹簧夹。
(4)提高铜片上白磷的温度并使水中白磷隔绝氧气
考点:铁生锈条件探究,空气中氧气含量探究,燃烧条件探究。

下列实验操怍能达到目的是
选项 | 实验目的 | 实验操作 |
A | 检验某未知溶液是否为碱溶液 | 溶液的pH |
B | 鉴别食盐水和氯化钙溶液 | 分别取两种溶液少量.通入CO2气体 |
C | 除去硫酸铜溶液中过量的硫酸 | 加入适量的NaOH溶液 |
D | 除去氢气中的HCl和H20蒸气 | 通过盛装生石灰颗粒的U形管 |
铬(Cr)是重要的金属材料,越来越受到人们的关注。某化学兴趣小组对Cr、Al、Cu的金属活动性顺序进行探究,过程如下:
【提出假设】对三种金属的活动性顺序提出三种可能的假设:
a.Al>Cr>Cu b.Cr>Al>Cu c. (1)
【设计实验】同温下,取大小相同的打磨过的金属薄片,分别投入到等体积等浓度的足量稀盐酸中,观察现象,记录如下:
金属 | Cr | Al | Cu |
与盐酸反应的现象 | 气泡产生缓慢,金属逐渐溶解 | 气泡产生剧烈,金属迅速溶解 | 无气泡产生,金属无变化 |
【控制实验条件】打磨三种金属的目的是 (2) ;
【得出结论】原假设中正确的是 (3) (填假设中a、b或c)。写出铬(铬与盐酸反应后显+2价)与盐酸反应的化学方程式 (4) 。
【结论应用】根据探究结果,在CuCl2和AlCl3的混合液中加入一定量的金属铬,充分反应后过滤.向滤出的固体中加入盐酸,无明显现象,则滤液中一定有的物质是 (5) 。
A和B可发生如下反应:3A+2B==A3B2,某学生做了3次该实验(每次均充分反应),反应前A和B的质量和都是10 g。有关实验数据见右表,x∶y的值可能为
序号 | 反应前 A的质量 | 反应前 B的质量 | 反应后A3B2 的质量 |
① | 8g | 2g | 6g |
② | 4g | 6g | 6g |
③ | xg | yg | 9g |
A.1︰1 B.2︰1 C.1︰4 D.3︰2