题目内容
氯酸钾与二氧化锰的混合物共28.4g,加热完全发生分解后剩余固体的质量为18.8g.
(1)生成氧气的质量为 g.
(2)剩余固体中二氧化锰的质量为多少?(第2小题写出解答步骤)
【考点】根据化学反应方程式的计算.
【专题】有关化学方程式的计算;有关化学方程式的计算.
【分析】(1)氯酸钾在二氧化锰催化下受热分解生成氯化钾和氧气,反应中二氧化锰为催化剂其质量在变化前后质量不变;由于反应产生气体氧气,根据质量守恒定律,完全反应前后固体物质的质量差即为放出氧气的质量;
(2)利用反应得到氧气的质量,根据反应的化学方程式,可计算生成氯化钾质量,进而可得混合物中二氧化锰的质量.
【解答】解:(1)氯酸钾在二氧化锰催化下受热分解生成氯化钾和氧气,反应中二氧化锰为催化剂其质量在变化前后质量不变;由于反应产生气体氧气,根据质量守恒定律,完全反应前后固体物质的质量差即为放出氧气的质量,依题意可知完全反应后生成氧气的质量为:28.4g﹣18.8g=9.6g;故填:9.6;
(2)设剩余固体中KCl质量为x,
2KClO3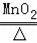
 2KCl+3O2↑
2KCl+3O2↑
149 96
x 9.6g
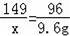

x=14.9g
剩余固体中二氧化锰的质量为:18.8g﹣14.9g=3.9g
答:剩余固体中二氧化锰的质量为3.9g.
【点评】根据质量守恒定律,由反应前后固体物质质量差即反应所产生氧气的质量是解题的关键,难度较大.

练习册系列答案
 春雨教育同步作文系列答案
春雨教育同步作文系列答案
相关题目


 B.
B.
 C.
C.
 D.
D.


 2KCl+3O2↑,如图表示一定质量的KClO3和MnO2固体混合物受热过程中,某变量y随时间的变化趋势,纵坐标表示的是( )
2KCl+3O2↑,如图表示一定质量的KClO3和MnO2固体混合物受热过程中,某变量y随时间的变化趋势,纵坐标表示的是( )