题目内容
12.构成的物质的微粒有分子、原子、离子等,如金刚石是由碳原子构成的;水是由水分子构成的;食盐固体是由钠离子和氯离子构成的.分析 构成物质的基本粒子有分子、原子和离子.根据金属、大多数固态非金属单质、稀有气体等由原子构成;有些物质是由分子构成的,气态的非金属单质和一般由非金属元素组成的化合物,如氢气、水等;有些物质是由离子构成的,一般是含有金属元素和非金属元素的化合物,如氯化钠,进行分析解答即可.
解答 解:构成物质的基本粒子有分子、原子和离子.金刚石属于固态非金属单质,是由碳原子直接构成的;水是由非金属元素组成的化合物,是由水分子构成;食盐固体是含有金属元素和非金属元素的化合物,食盐固体是由钠离子和氯离子构成的.
故答案为:离子;碳原子;水分子;钠离子和氯离子.
点评 本题难度不大,主要考查了构成物质的微观粒子方面的知识,对物质进行分类与对号入座、掌握常见物质的粒子构成是正确解答本题的关键.

练习册系列答案
相关题目
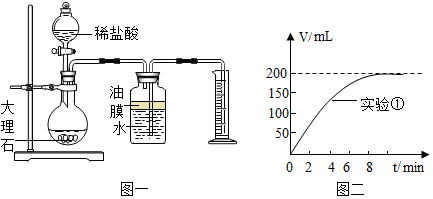
2.在制取CO2的实验中,小科发现质量相同而粗细不同的大理石与盐酸反应,CO2的产生速度细的比粗的快得多.经思考后,小科设计了如下实验(每次实验均用1g大理石,20mL盐酸)
(1)为了比较反应速度,设计如图一所示装置,其中量筒的作用是通过观察单位时间内排入量筒中水的体积来判断反应速率;
(2)实验中CO2体积随时间的变化关系如图二所示,请将实验2中CO2体积随时间变化的曲线画在图二中.
(3)已知20℃该气压下CO2气体密度约1.98g/L,求大理石中CaCO3的质量分数?(详细计算过程)(C-12 O-16 Ca-40)
| 实验序号 | 温度(℃) | 大理石颗粒 | 盐酸质量分数(%) | 实验目的 |
| 1 | 20 | 粗 | 5 | 探究大理石和盐酸的反应速度与石灰石颗粒大小的关系 |
| 2 | 20 | 细 | 5 |
(2)实验中CO2体积随时间的变化关系如图二所示,请将实验2中CO2体积随时间变化的曲线画在图二中.

(3)已知20℃该气压下CO2气体密度约1.98g/L,求大理石中CaCO3的质量分数?(详细计算过程)(C-12 O-16 Ca-40)
3.20℃时,将30克某物质投入到50克水中充分溶解,还有10克未溶解,问20℃时,该物质的溶解度为( )
| A. | 50克 | B. | 30克 | C. | 40 | D. | 40克 |
20.金属钴(Co)与铁的化学性质相似,都能与稀盐酸反应,在化合物中钴元素常显+2,+3价,下列说法正确的是( )
| A. | CoCl3读作“氯化亚钴” | |
| B. | 补充钴元素可以防止贫血 | |
| C. | 金属铜不能与CoCl2溶液发生反应 | |
| D. | CoCl2中钴元素的质量分数约为33.3% |
17.如表是某成年男子血液的化验结果.根据表中的数据回答:
(1)依据化验项目第②项判断此人有炎症,原因在于白细胞数目高出正常值.
(2)依据化验项目第①项判断此人患有贫血.请在下列四项中选择:他应该多吃含B、D丰富的食品.(可多选)
A.钙 B.铁 C.维生素B1 D.蛋白质.
| 化验项目 | 正常情况 | 化验结果 | |
| 血液 | ①血红蛋白 | 120~150克/升 | 100克/升 |
| ②白细胞 | 4×109~10×109个/升 | 16×109个/升 | |
| ③血清 | 含抗A凝集素 |
(2)依据化验项目第①项判断此人患有贫血.请在下列四项中选择:他应该多吃含B、D丰富的食品.(可多选)
A.钙 B.铁 C.维生素B1 D.蛋白质.
2.小明为了测定某石灰石中碳酸钙的质量分数,用如图装置进行如下实验: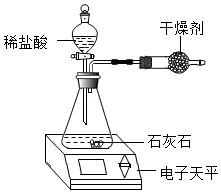
①取研碎后的石灰石2.5克,倒入气密性良好的锥形瓶中,然后在分液漏斗中加入适量的稀盐酸,置于电子天平上测出装置总质量.
②打开活塞,滴入足量稀盐酸后关闭活塞,待气泡不再冒出时,测出反应后装置总质量.
③整理相关数据如下表,计算出石灰石中碳酸钙的质量分数.
(1)该实验中,对装置中的固态干燥剂的性质有何要求?能吸收水不能吸收二氧化碳.
(2)结合表中数据,计算该石灰石中碳酸钙的质量分数.(CaCO3+2HCl=CaCl2+H2O+CO2↑,石灰石中的其它成分不与盐酸反应)
(3)实验后小明认真反思觉得该实验测得的石灰石中碳酸钙的质量分数比实际值会偏小(填“偏大”、“偏小”或“不变”),理由是反应后有部分二氧化碳残留在锥形瓶中使测量得到的二氧化碳的质量变小,故计算得到的碳酸
钙的质量也变小.

①取研碎后的石灰石2.5克,倒入气密性良好的锥形瓶中,然后在分液漏斗中加入适量的稀盐酸,置于电子天平上测出装置总质量.
②打开活塞,滴入足量稀盐酸后关闭活塞,待气泡不再冒出时,测出反应后装置总质量.
③整理相关数据如下表,计算出石灰石中碳酸钙的质量分数.
| 反应前总质量(克) | 275.58 |
| 反应后总质量(克) | 274.70 |
| 反应前后质量差(克) | 0.88 |
(2)结合表中数据,计算该石灰石中碳酸钙的质量分数.(CaCO3+2HCl=CaCl2+H2O+CO2↑,石灰石中的其它成分不与盐酸反应)
(3)实验后小明认真反思觉得该实验测得的石灰石中碳酸钙的质量分数比实际值会偏小(填“偏大”、“偏小”或“不变”),理由是反应后有部分二氧化碳残留在锥形瓶中使测量得到的二氧化碳的质量变小,故计算得到的碳酸
钙的质量也变小.
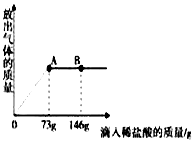 在一烧杯中盛有22.3gNa2CO3和NaCl组成的固体混合物,加入109.1g水溶解,制成溶液.向其中滴加溶质质量分数10%的稀盐酸,放出气体的总质量与所滴入稀盐酸的质量关系如图所示,请回答问题:
在一烧杯中盛有22.3gNa2CO3和NaCl组成的固体混合物,加入109.1g水溶解,制成溶液.向其中滴加溶质质量分数10%的稀盐酸,放出气体的总质量与所滴入稀盐酸的质量关系如图所示,请回答问题: