题目内容
3.坐落于扬州宝应的江苏宝胜集团是一家以生产电缆类产品为主的国家大型企业.在电缆生产过程中,不可避免地会产生一定量的含铜废料(如:零碎电缆).某化学兴趣小组的四位同学得知这一情况后,围绕“从含铜废料中回收铜”提出了各自的看法.甲同学根据已学知识,提出了一套回收方案: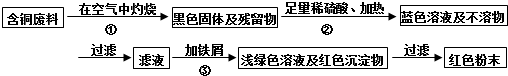
乙同学在查阅资料后得知:在通入空气并加热的条件下,铜可与稀硫酸在溶液中发生反应(方程式为:2Cu+2H2SO4+O2$\frac{\underline{\;\;△\;\;}}{\;}$2CuSO4+2H2O),于是他提出了另一套方案:
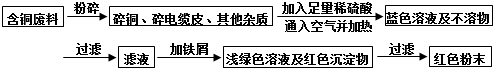
(1)环保角度对两套方案的不同部分进行比较,你认为乙(填“甲”或“乙”)的方案更合理.理由是:甲方案第一步灼烧会产生污染空气的气体,粉尘,烟雾.
(2)认为,无论是甲还是乙的方案,在“加铁屑”这一步时,应该加入略过量的铁屑.你认为丙这么说的道理是确保CuSO4用完或将铜完全置换.丁又提出了疑问:“如果铁过量,剩余的铁会混在红色粉末中,该怎么处理呢?”.请提出你的想法:将所得的铜粉酸洗后再洗涤,干燥 或 过滤前先加适量的酸除去剩余的铁粉.
(3)后,老师肯定了同学们的积极思考,但同时指出:方案最后一步所得浅绿色滤液晶后,会得到一种俗称“绿矾”的工业产品,可增加经济效益.请写出使“绿矾”结晶两种可能方法:蒸发结晶、降温结晶(“绿矾”溶解度随温度升高而增大).如果直接排放掉滤液,不仅造成了浪费,还会造成水污染或环境污染.
分析 铜能与氧气反应生成氧化铜,生成的氧化铜可以与酸反应生成盐和水,在金属活动性顺序中,氢前的金属能与酸反应生成盐和氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来,要回收铜可以加入活动性比铜强的金属,然后结合结晶的方法进行分析.
解答 解:(1)从环保角度对两套方案的不同部分进行比较,甲方案第一步灼烧会产生污染空气的气体,粉尘,烟雾,由此可知乙的方案更合理,
故答案为:乙;甲方案第一步灼烧会产生污染空气的气体,粉尘,烟雾;
(3)加入略过量的铁屑,是将硫酸铜全部置换出来;如果铁过量,会混在红色粉末中,可以加入适量的酸除去剩余的铁屑,
故答案为:确保CuSO4用完或将铜完全置换;将所得的铜粉酸洗后再洗涤,干燥 或 过滤前先加适量的酸除去剩余的铁粉;
(4)结晶的方法有:冷却热饱和溶液和蒸发溶剂法,即蒸发结晶和降温结晶;直接排放掉滤液,不仅造成了浪费,还会造成环境污染或水污染;
故答案为:蒸发结晶、降温结晶;造成水污染或环境污染.
点评 本题探讨了“从含铜废料中回收铜”的有关问题,设计了不同的方案,并进行评价,考察了考生的思考、探讨、评价等诸多能力.

练习册系列答案
相关题目
17.下列说法正确的是( )
| A. | 按质量分数计算,空气中氮气约点78% | |
| B. | 电子能量越高离原子核越近 | |
| C. | 空气是重要的自然资源 | |
| D. | 稀有气体不与任何物质发生反应 |
18.实验室里有两瓶失去标签的白色粉末,只知它们分别是氯化钠(NaCl)和碳酸钙(CaCO3)(难溶于水),请设计一个实验方案,将它们区分开来.将实验步骤、预期现象与结论填写在下列表格中.
| 实验步骤 | 预期现象与结论 |
8.下列物质能在pH=1的溶液中共存且能形成有色溶液的是( )
| A. | (NH4)2SO4、FeCl3、NaNO3、K2SO4 | B. | KOH、KNO3、NaCl、FeCl2 | ||
| C. | MgSO4、NaCl、HNO3、K2CO3 | D. | Ba(OH)2、CuSO4、MgCl2、H2SO4 |
11.图为某反应的微观示意图,下列说法错误的是( )
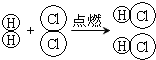

| A. | 反应物氢气、氯气与生成物氯化氢的质量比为2:71:36.5 | |
| B. | 该反应属于化合反应 | |
| C. | 该生成物溶于水后,所得溶液pH<7 | |
| D. | 化学反应前后原子的种类和数目不变 |
 下列仪器室化学实验常用的仪器.
下列仪器室化学实验常用的仪器.