题目内容
15.阅读下面科普短文酸雨是指pH小于5.6的雨雪或其他形式的降水.酸雨主要是人为的向大气中排放大量酸性物质所造成的.雨、雪等在形成和降落过程中,吸收并溶解了空气中的二氧化硫或氮氧化物等物质,形成了pH低于5.6的酸性降水.
酸雨中的阴离子主要是硝酸根和硫酸根离子,根据两者在酸雨样品中的浓度可以判定降水的主要影响因素是二氧化硫还是氮氧化物.二氧化硫主要是来自于矿物燃料(如煤)的燃烧,氮氧化物主要是来自于汽车尾气等污染源.
含有硫的煤燃烧生成二氧化硫,二氧化硫和水作用生成亚硫酸(H2SO3),H2SO3在空气中被氧化成硫酸.
雷雨闪电时,大气中也会产生少量硝酸.闪电时,氮气与氧气化合生成一氧化氮(NO),NO不稳定,在空气中被氧化成二氧化氮(NO2).NO2是一种红棕色、具有刺激性气味的气体,它可和水作用生成硝酸.
酸雨对环境、工农业生产、建筑、森林、植物等危害巨大.
依据文章内容,回答下列问题:
(1)NO2的物理性质红棕色、具有刺激性气味的气体.
(2)NO与NO2化学性质不同的原因是分子(组成和结构)不同.
(3)H2SO3在空气中转化为硫酸的化学方程式为O3+2H2SO3═2H2SO4 .
(4)氮气与氧气化合生成一氧化氮反应的化学方程式为N2+O2$\frac{\underline{\;放电\;}}{\;}$2NO.
(5)你认为防治酸雨的方法是开发新能源;使用燃煤脱硫技术,减少二氧化硫排放;工业尾气处理后再排放;少开车,多乘坐公共交通工具出行;使用天然气等较清洁能源,少用煤.
分析 (1)根据题中信息分析解答;
(2)根据分子是保持物质化学性质的微粒解答;
(3)根据二氧化硫与雨水反应生成亚硫酸,亚硫酸被空气中的氧气氧化成硫酸写化学方程式;
(4)根据氮气与氧气化合生成一氧化氮,写出反应的化学方程式解答;
(5)根据酸雨的成因回答.
解答 解:
(1)根据题中信息可知:NO2的物理性质是红棕色、具有刺激性气味的气体;
(2)NO与NO2化学性质不同的原因是分子(组成和结构)不同;
(3)H2SO3在空气中转化为硫酸的化学方程式为:O3+2H2SO3═2H2SO4 ;
(4)氮气与氧气化合生成一氧化氮,反应的化学方程式为:N2+O2$\frac{\underline{\;放电\;}}{\;}$2NO;
(5)减少酸雨主要是减少二氧化硫的排放,如开发新能源;使用燃煤脱硫技术,减少二氧化硫排放;工业尾气处理后再排放;少开车,多乘坐公共交通工具出行;使用天然气等较清洁能源,少用煤.
答案:
(1)红棕色、具有刺激性气味的气体;
(2)分子(组成和结构)不同;
(3)O3+2H2SO3═2H2SO4;
(4)N2+O2$\frac{\underline{\;放电\;}}{\;}$2NO;
(5)开发新能源;使用燃煤脱硫技术,减少二氧化硫排放;工业尾气处理后再排放;少开车,多乘坐公共交通工具出行;使用天然气等较清洁能源,少用煤.
点评 本题考查酸雨的形成过程,通过对酸雨形成的了解,可以使我们更好的了解如何防止酸雨.

练习册系列答案
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目
3.下列实验操作中,正确的是( )
| A. | 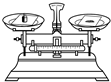 称量固体 | B. |  点燃酒精灯 | C. |  取用固体粉末 | D. | 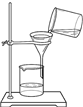 过滤 |
7.下列不属于氧气用途的是( )
| A. | 灭火 | B. | 宇宙航行 | C. | 气焊 | D. | 潜水 |
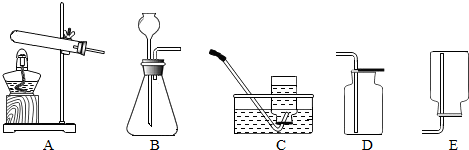
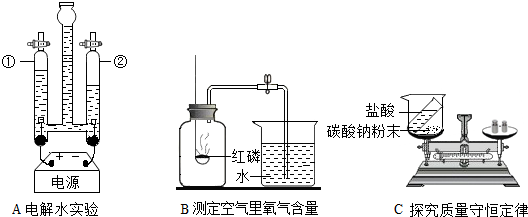

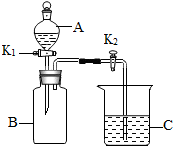 同学们利用如图做了如下实验(A、B、C中盛放有不同的药品):
同学们利用如图做了如下实验(A、B、C中盛放有不同的药品):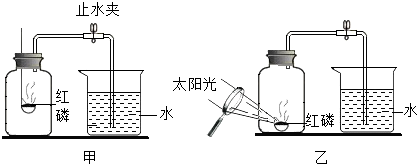
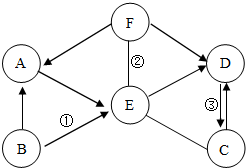 A~F均为生活中常见的物质.其中A与B的元素组成相同,C与D的元素组成相同;A、B、C、D的类别相同,C、D、E、F在常温下的状态相同.其物质间的转化关系如图所示,图中“--”表示两端的物质能发生化学反应;“”表示物质间存在转化关系,其余反应条件、部分反应物和生成物均已略去.试推断:
A~F均为生活中常见的物质.其中A与B的元素组成相同,C与D的元素组成相同;A、B、C、D的类别相同,C、D、E、F在常温下的状态相同.其物质间的转化关系如图所示,图中“--”表示两端的物质能发生化学反应;“”表示物质间存在转化关系,其余反应条件、部分反应物和生成物均已略去.试推断: