题目内容
用棕色试剂瓶保存AgNO3溶液,AgNO3见光分解时放出刺激性气味的气体可能是( )
| A、SO2 |
| B、NO2 |
| C、NH3 |
| D、N2 |
考点:质量守恒定律及其应用
专题:化学用语和质量守恒定律
分析:根据质量守恒定律:化学反应前后元素的种类不变,可初步的判断生成物是什么,根据反应前AgN03中存在银、氮、氧三种元素,故反应后的生成物中不可能有SO2和NH3.然后根据题中“AgNO3受热分解,放出的有刺激性气味的气体”,放出有刺激性气味的气体可排除氮气.
解答:解:
A、AgN03中不含有硫元素,根据质量守恒定律,不可能是S02,故A错误;
B、AgN03中存在银、氮、氧三种元素,N02又有刺激性气味,所以有可能,故B正确;
C、AgN03中不含有氢元素,根据质量守恒定律,不可能是NH3,故C错误;
D、N2无刺激性气味,不可能含有,故D错误;
故选:B.
A、AgN03中不含有硫元素,根据质量守恒定律,不可能是S02,故A错误;
B、AgN03中存在银、氮、氧三种元素,N02又有刺激性气味,所以有可能,故B正确;
C、AgN03中不含有氢元素,根据质量守恒定律,不可能是NH3,故C错误;
D、N2无刺激性气味,不可能含有,故D错误;
故选:B.
点评:该题主要考查了质量守恒定律的应用,该题还要求学生要善于从题中挖掘出有用的解题信息(例如分解放出有刺激性气味的气体),以及要求学生要学会用排除法做选择题.

练习册系列答案
相关题目
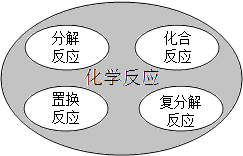 下列化学反应属于如图关系图中阴影部分的是( )
下列化学反应属于如图关系图中阴影部分的是( )A、CuO+CO
| ||||
B、2H2O
| ||||
| C、CaO+H2O═Ca(OH)2 | ||||
| D、2NaOH+H2SO4═Na2SO4+2H2O |
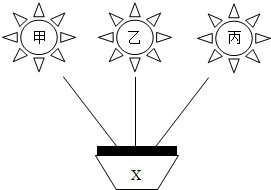 化学变化多姿多彩,美丽如花,图中甲、乙、丙分别是CuSO4溶液、O2、硫酸中的一种,甲、乙、丙均能与x发生化学反应,则x是( )
化学变化多姿多彩,美丽如花,图中甲、乙、丙分别是CuSO4溶液、O2、硫酸中的一种,甲、乙、丙均能与x发生化学反应,则x是( )| A、Fe |
| B、Fe2O3 |
| C、氯化钡 |
| D、碳酸钠 |
某化学反应过程的微观示意图如下:下列说法错误的是( )
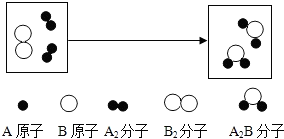

| A、上述反应的化学方程式可表示为:2A+B=A2B |
| B、原子是化学变化中的最小粒子 |
| C、元素的种类、原子的数目在化学变化前后不变 |
| D、在化学变化中分子分成原子,原子又重新组合成新物质的分子 |
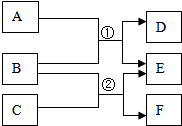 A-F表示初中化学常见的物质,A和B,B和C都能发生反应,且都只能生成两种产物,它们之间的转化关系如图所示.
A-F表示初中化学常见的物质,A和B,B和C都能发生反应,且都只能生成两种产物,它们之间的转化关系如图所示.