题目内容
11.将一定量的锌粉投入硝酸钾、硝酸银、硝酸镁、硝酸铜的混合溶液中,充分反应后过滤.若滤液中有硝酸银,则滤渣中一定有的物质是Ag (填化学式):若滤渣中只有Cu、Ag,则滤液中一定没有的溶质是AgNO3(填化学式).分析 根据锌的金属活动性比银、铜都强,没有镁、钾活泼,所以将一定量的锌粉投入硝酸钾、硝酸银、硝酸镁、硝酸铜的混合溶液中,会与硝酸铜、硝酸银反应,不会与硝酸钾、硝酸镁反应,锌会先于硝酸银反应再与硝酸铜反应进行分析.
解答 解:锌的金属活动性比银、铜都强,没有镁、钾活泼,所以将一定量的锌粉投入硝酸钾、硝酸银、硝酸镁、硝酸铜的混合溶液中,会与硝酸铜、硝酸银反应,不会与硝酸钾、硝酸镁反应,锌会先于硝酸银反应再与硝酸铜反应,所以若滤液中有硝酸银,说明银没有被置换完,所以滤渣中一定有的物质是Ag,若滤渣中只有Cu、Ag,说明锌与硝酸铜发生了反应,但是无法判断反应的程度,所以滤液中一定没有的溶质是AgNO3.
故答案为:Ag,AgNO3.
点评 本题主要考查了对金属活动性顺序的灵活应用,只有活动性强的金属可以把活动性弱的金属从盐溶液中置换出来,培养学生分析问题、解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.下来变化中属于化学变化的是( )
| A. | 蜡烛燃烧 | B. | 汽车爆胎 | C. | 蔬菜榨汁 | D. | 玻璃破碎 |
10.向一定量的AgNO3与Cu(NO3)2的混合溶液中加入一定量的锌粉,充分反应后过滤.分析判断下列说法正确的是( )
| A. | 滤渣中一定有Zn,可能有Ag | |
| B. | 滤渣中一定有Cu、Ag,可能有Zn | |
| C. | 滤液中只有Zn(NO3)2 | |
| D. | 滤液中一定有Zn(NO3)2,可能有Cu(NO3)2 |
6.人类生产、生活离不开金属材料.
(1)人们习惯上把金、银、铜、铁、锡五种金属称为“五金”,在“五金”顺序中把金属铁的位置移到后面正好符合由弱到强的顺序.
(2)铜也容易生锈,铜锈的主要成分是碱式碳酸铜[化学式为Cu2(OH)2CO3],是铜与空气中的氧气、水和二氧化碳共作用的结果.
(3)合金是由两种或两种以上的金属(或金属与非金属)熔合而成的具有金属特性的物质.一般来说,合金的熔点低于任何一种组成金属的熔点.下表是一些金属的熔点数据:
保险丝由铋、铅、锡、镉组成,其熔点最高不超过231.9℃
(4)实验室中有铁、铜、锌三种金属,某同学想用实验的方法探究铁、铜、锌三种金属的活泼性顺序,若只提供一种溶液来完成该实验,他所选择的试剂是FeSO4溶液,写出反应的化学方程式:FeSO4+Zn=ZnSO4+Fe.
(1)人们习惯上把金、银、铜、铁、锡五种金属称为“五金”,在“五金”顺序中把金属铁的位置移到后面正好符合由弱到强的顺序.
(2)铜也容易生锈,铜锈的主要成分是碱式碳酸铜[化学式为Cu2(OH)2CO3],是铜与空气中的氧气、水和二氧化碳共作用的结果.
(3)合金是由两种或两种以上的金属(或金属与非金属)熔合而成的具有金属特性的物质.一般来说,合金的熔点低于任何一种组成金属的熔点.下表是一些金属的熔点数据:
| 金属 | 铜 | 锌 | 锡 | 铅 | 铋 | 镉 |
| 熔点/℃ | 108.3 | 419.6 | 231.9 | 327.5 | 271.3 | 320.9 |
(4)实验室中有铁、铜、锌三种金属,某同学想用实验的方法探究铁、铜、锌三种金属的活泼性顺序,若只提供一种溶液来完成该实验,他所选择的试剂是FeSO4溶液,写出反应的化学方程式:FeSO4+Zn=ZnSO4+Fe.
16.下列关于水的叙述,不正确的是( )
| A. | 蒸馏可以将硬水转化为软水 | |
| B. | 电解水时正负两极产生的气体质量之比为1:2 | |
| C. | 盐酸和稀硫酸的溶剂都是水 | |
| D. | 过量使用农药、化肥会造成水体污染 |
3.下列化学家与其做出贡献的叙述对应一致的是( )
| A. |  法国-拉瓦锡发现质量守恒定律 | |
| B. |  中国-侯德榜发明联合制烧碱法 | |
| C. |  中国--张青莲发现原子的结构 | |
| D. |  俄国--门捷列夫解释水不是一种元素组成的 |
1.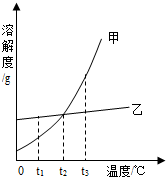 如图是甲、乙两种固体物质的溶解度曲线图.下列说法中正确的是( )
如图是甲、乙两种固体物质的溶解度曲线图.下列说法中正确的是( )
 如图是甲、乙两种固体物质的溶解度曲线图.下列说法中正确的是( )
如图是甲、乙两种固体物质的溶解度曲线图.下列说法中正确的是( )| A. | t2℃时,甲、乙两种物质溶液的溶质质量分数一定相等 | |
| B. | t1℃时,把甲的不饱和溶液变为饱和溶液,溶剂质量一定不变 | |
| C. | 若甲中混有少量乙,可采用蒸发结晶的方法提纯甲 | |
| D. | t3℃时,将甲、乙的饱和溶液都蒸发掉 10g水,析出甲的晶体质量比析出乙的晶体质量大 |
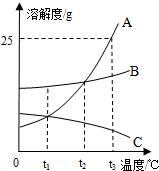 A、B、C三种固体物质在水中的溶解度曲线如图所示,请回答:
A、B、C三种固体物质在水中的溶解度曲线如图所示,请回答: