题目内容
黄铜是铜锌合金,可用于制造仪表,机器零件和日用品.为了测定某黄铜样品中锌的质量分数,甲、乙、丙三位同学分别进行如下实验,实验数据如下(烧杯质量均为56g).请计算:
(1)从表格三次实验中对比可发现: 同学取用的稀盐酸和样品恰好完全反应,他得到的氢气质量是 ;
(2)求实验中所加稀盐酸中溶质的质量分数.
| 甲 | 乙 | 丙 | |
| 烧杯+稀盐酸 | 139 | 129 | 129 |
| 加入黄铜样品 | 20 | 24 | 20 |
| 充分反应后,烧杯+剩余物质 | 158.8 | 152.8 | 148.8 |
(2)求实验中所加稀盐酸中溶质的质量分数.
考点:根据化学反应方程式的计算,有关溶质质量分数的简单计算
专题:综合计算(图像型、表格型、情景型计算题)
分析:(1)根据甲、乙、丙三次放出氢气的质量都是0.2g进行解答;
(2)根据氢气的质量利用化学方程式求出参见反应的盐酸中溶质的质量,进而求出所加稀盐酸中溶质的质量分数即可.
(2)根据氢气的质量利用化学方程式求出参见反应的盐酸中溶质的质量,进而求出所加稀盐酸中溶质的质量分数即可.
解答:解:(1)甲、乙、丙三次放出氢气的质量都是0.2g,甲中稀盐酸的质量多,乙中黄铜样品质量多,所以丙同学取用的稀盐酸和样品恰好完全反应,他制取的氢气的质量是129g+20g-148.8g=0.2g;故填:丙;0.2g;
(2)设参见反应的盐酸中溶质的质量为x
丙中盐酸的质量=129g-56g=73g
Zn+2HCl═ZnCl2+H2↑
73 2
x 0.2g
=
x=7.3g
所加稀盐酸中溶质的质量分数:
×100%=10%
答:所加稀盐酸中溶质的质量分数为10%.
(2)设参见反应的盐酸中溶质的质量为x
丙中盐酸的质量=129g-56g=73g
Zn+2HCl═ZnCl2+H2↑
73 2
x 0.2g
| 73 |
| x |
| 2 |
| 0.2g |
x=7.3g
所加稀盐酸中溶质的质量分数:
| 7.3g |
| 73g |
答:所加稀盐酸中溶质的质量分数为10%.
点评:本题考查了混合金属中金属含量的测定,完成此题,可以依据金属与酸的反应及其反应的化学方程式进行.

练习册系列答案
相关题目
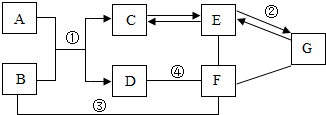 A~G是初中化学常见的物质.其中B是一种红色粉末,A、C是常见的气体,E在工业上常用于造纸、制洗涤剂、洗衣服、玻璃等,F是由两种元素组成的,E和G属于不同类别的物质.如图中“--”表示相邻的两种物质间能发生化学反应.“→”表示物质间存在转化关系(部分反应物、生成物和反应条件已略去),请回答下列问题:
A~G是初中化学常见的物质.其中B是一种红色粉末,A、C是常见的气体,E在工业上常用于造纸、制洗涤剂、洗衣服、玻璃等,F是由两种元素组成的,E和G属于不同类别的物质.如图中“--”表示相邻的两种物质间能发生化学反应.“→”表示物质间存在转化关系(部分反应物、生成物和反应条件已略去),请回答下列问题: