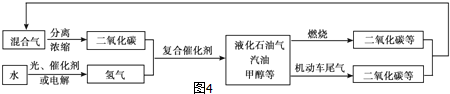
题目内容
19.具有10个电子的n价金属离子,其中子数为N,质子数为Z.N和Z的关系是N=Z+1,则该金属的近似相对原子质量是( )| A. | N+Z+10 | B. | N+Z+1 | C. | N+Z+n | D. | 2n+21 |
分析 根据题意,具有10个电子的n价金属离子,化合价的数值等于离子所带电荷的数值,且符号一致,金属离子带正电荷,则n价金属离子是钙金属原子失去n个电子得到的,即该金属原子的核外电子数为10+n;据此结合原子中核内质子数=核外电子数、相对原子质量=质子数+中子数,结合题意进行分析解答.
解答 解:具有10个电子的n价金属离子,化合价的数值等于离子所带电荷的数值,且符号一致,金属离子带正电荷,则n价金属离子是钙金属原子失去n个电子得到的,即该金属原子的核外电子数为10+n;原子中核内质子数=核外电子数,则10+n=Z.
相对原子质量=质子数+中子数,由题意,其中子数为N,质子数为Z,N和Z的关系是N=Z+1,该金属的近似相对原子质量为N+Z=Z+1+Z=2Z+1=2×(10+n)+1=2n+21.
故选:D.
点评 本题难度不大,掌握化合价的数值等于离子所带电荷的数值且符号一致、原子中核内质子数=核外电子数、相对原子质量=质子数+中子数是正确解答本题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
9.课外小组同学进一步研究铁与氧气的反应.
【提出问题】铁丝燃烧时为什么会有“火星四射”的现象?
【查阅资料】生铁中含有一定量的碳.铁丝燃烧时“火星四射”现象与铁丝中含碳量有关.
【进行实验】探究铁丝在氧气中燃烧时“火星四射”的现象与其含碳量的关系.
【提出问题】纯铁在氧气中燃烧溅落的“黑色固体”是什么?
【查阅资料】
①自然界中铁的氧化物主要是Fe3O4和Fe2O3两种(FeO易被氧化)
②铁的氧化物均能溶于酸溶液
③单质铁与稀盐酸反应的化学方程式为:Fe+2HCl═FeCl2+H2↑.
【进行实验】测定黑色固体的成分.
【实验反思】
同学们认为铁丝燃烧的现象还与氧气的浓度有关,所以想收集不同浓度的氧气进行相关实验.若用排水集气法收集一瓶体积分数约为60%的氧气,预先应向容积为250mL的集气瓶中加水,水的体积约为125mL.
【提出问题】铁丝燃烧时为什么会有“火星四射”的现象?
【查阅资料】生铁中含有一定量的碳.铁丝燃烧时“火星四射”现象与铁丝中含碳量有关.
【进行实验】探究铁丝在氧气中燃烧时“火星四射”的现象与其含碳量的关系.
| 实验 | 现象 | 解释与结论 |
| 实验1:取直径0.20mm、含碳0.1% 的铁丝,在氧气中燃烧 | 零星的火星四射 | ①铁燃烧的化学方程式是3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4. ②0.20mm的铁丝在氧气中燃烧,“火星四射”与其含碳量的关系为含碳量越高,火星四射的现象越明显 |
| 实验2:取直径0.20mm、含碳0.32%的铁丝,在氧气中燃烧 | 较明显的火星四射 | |
| 实验3:取直径0.20mm、含碳0.52%的铁丝,在氧气中燃烧 | 明显的火星四射 |
【查阅资料】
①自然界中铁的氧化物主要是Fe3O4和Fe2O3两种(FeO易被氧化)
②铁的氧化物均能溶于酸溶液
③单质铁与稀盐酸反应的化学方程式为:Fe+2HCl═FeCl2+H2↑.
【进行实验】测定黑色固体的成分.
| 实验 | 现象及数据 | 解释与结论 |
| 实验4:将冷却后的黑色固体碾碎,装入试管,加入稀盐酸 | 现象是有气泡产生 | 铁燃烧时溅落下来的黑色 固体中含有铁 |
| 实验5:取2.8g纯铁在氧气中燃烧,收集溅落的黑色固体,干燥并称其质量 | 黑色固体质量为3.44g | 黑色固体的组成及质量 为Fe1.12g,Fe3O42.32g |
同学们认为铁丝燃烧的现象还与氧气的浓度有关,所以想收集不同浓度的氧气进行相关实验.若用排水集气法收集一瓶体积分数约为60%的氧气,预先应向容积为250mL的集气瓶中加水,水的体积约为125mL.
10.科学家研制出高灵敏度的CO探测器,通过颜色变化可探测空气中是否含有CO.下列有关说法不正确的是( )
| A. | CO的物理性质是无色、无味、具有可燃性 | |
| B. | 该探测器可警示室内燃煤取暖是否安全 | |
| C. | CO中毒时,应将病人迅速转移到室外 | |
| D. | CO有毒,是因其易与人体中的血红蛋白结合,影响血液对氧气的输送 |
7.根据三种不同的原子(如表所示),则下列说法正确的是( )
| A 原子 | B原子 | C原子 | |
| 质子数 | 8个 | 8个 | 7个 |
| 中子数 | 8个 | 9个 | 7个 |
| A. | A和C是同一种元素 | B. | B和C核外电子数相等 | ||
| C. | A和B是同种元素 | D. | A和B的核电荷数不同 |
6.科学实验要规范操作,下列初中科学实验操作你认为正确的是( )
| A. | 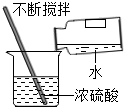 稀释浓硫酸 | B. | 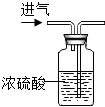 干燥氧气 | C. | 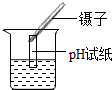 测定某溶液的pH | D. |  检查气密性 |
 某同学对蜡烛(主要成分是石蜡)及其燃烧进行了如下探究.请填写下列空格.
某同学对蜡烛(主要成分是石蜡)及其燃烧进行了如下探究.请填写下列空格.