题目内容
14. (1)用铜制电线主要是利用铜具有良好的延展性和导电性.
(1)用铜制电线主要是利用铜具有良好的延展性和导电性.(2)工业炼铁的化学反应方程式为:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
(3)在硫酸铜和硫酸亚铁的混合溶液中加入一定量的锌粉,充分反应后过滤,向滤渣中滴加稀硫酸,无气泡产生.则滤渣中的金属是铜(Cu),滤液中溶质的组成是ZnSO4、FeSO4;ZnSO4、FeSO4和CuSO4(写出所有可能).
(4)将质量相等的锌粉和铁粉,分别放入两个烧杯中,再分别倒入质量相等、溶质的质
量分数相同的稀盐酸,充分反应,生成氢气的质量(m)随反应时间(t)变化的曲线如图所示.下列说法正确的是CD(填字母序号).
A.消耗两种金属的质量相等 B.两烧杯中金属都没有剩余
C.两烧杯中稀盐酸都没有剩余 D.曲线a表示锌和稀盐酸的反应.
分析 (1)根据铜的性质和用途来分析;
(2)根据炼铁的原理写出反应的方程式;
(3)由金属活动性顺序表可知:锌>铁>H>铜,根据这一活动强弱关系,分析实验中的实验现象,对反应后所得固体和溶液进行组成的推断;
(4)A.根据计算的分析如果锌、铁反应的质量相等,则产生的氢气一定不等;
B.由图象可知生成的氢气相等,故同质量金属与酸反应生成氢气较多的金属一定有剩余,据此解答;
C.根据生成的氢气质量相等,所以可知盐酸均反应完;
D.锌的活动性比铁的活动性强,等质量的金属,锌反应的时间短,据此分析解答.
解答 解:(1)铜能制导线,利用了铜的导电性;
(2)炼铁的原理就是利用一氧化碳与氧化铁反应,反应的方程式是:3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;
(3)滤渣加入稀硫酸无气泡产生,证明滤渣中只有铜,一定没有锌和铁,故加入的锌有可能没有将铜完全置换出来,也可能恰好将铜完全置换出来,则滤液的组成有两种可能:锌将铜恰好完全置换出来时,溶质是ZnSO4、FeSO4;若锌没有将铜完全置换出来,则溶质是ZnSO4、FeSO4和CuSO4.
(4)A.由以上的分析可知同质量的锌和铁与足量的稀硫酸反应时,铁生成的氢气多,故消耗两种金属的质量相等则产生的氢气一定不等,故说法错误;
B.由图象可知生成的氢气相等,故同质量金属与酸反应生成氢气较多的金属一定有剩余,由于氢气的质量=$\frac{金属的化合价}{金属的相对原子质量}$×金属的质量,所以可知铁一定有剩余,故说法错误;
C.由图象可知生成的氢气相等,由B的分析可知铁一定有剩余,故两盐酸均反应完全反应,只有这样生成的氢气才可能相等;故说法正确;
D.因为锌的活动性比铁的活动性强,等质量的金属,锌反应的时间短,曲线a表示锌和稀硫酸的反应,故说法正确.
故答案为:(1)导电;(2)3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2;(3)铜(Cu);ZnSO4、FeSO4;ZnSO4、FeSO4和CuSO4;
(4)C、D
点评 金属与盐溶液的混合物发生置换反应时,首先和活动性最弱的金属的盐反应,待该完全反应后再和余下盐溶液中金属活动性最弱的盐继续反应,最后置换出的金属则是相对较强的金属.

| A. | 用食盐腌渍菜、鱼、肉、蛋的方法可以延长食物的保存时间 | |
| B. | 用洗涤剂乳化油脂的方法除去餐具上的油污 | |
| C. | 用喷漆的方法防止自行车链条锈蚀 | |
| D. | 用沉淀、过滤、吸附等净化方法,可以使浑浊的水变澄清 |
| A. | 汽油和洗涤剂除油污的原理相同 | |
| B. | 空气、糖水、高锰酸钾都属于混合物 | |
| C. | 纯碱、烧碱都属于碱 | |
| D. | 只有当两种化合物互相交换成分,生成物中有沉淀或有气体或有水生成时,复分解反应才可以发生 |
| A. | 氮肥 | B. | 钾肥 | C. | 磷肥 | D. | 复合肥 |
| A. | 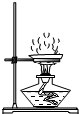 蒸发食盐水 | B. |  称量氢氧化钠 | C. |  稀释浓硫酸 | D. |  检验装置气密性 |
| A. | 氮原子 | B. | 氧原子 | C. | 氢原子 | D. | 碳原子 |
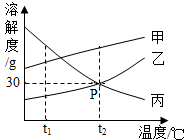 甲、乙、丙三种物质的溶解度曲线如图所示,请根据图回答下列有关问题:
甲、乙、丙三种物质的溶解度曲线如图所示,请根据图回答下列有关问题: