题目内容
17.在托盘天平的两盘分别放入质量相等的烧杯,烧杯中各盛放100g溶质质量分数为7.3%的稀盐酸,向两个烧杯中同时放入下列物质,反应停止后天平一定不平衡的是( )| A. | 2.4g镁 2.4g钙 | B. | 5.6g铁 5.6g锌和镁的混合物 | ||
| C. | 10g碳酸钙 5.6g氧化钙 | D. | 8.4gMg(OH)2 8.4gMg2CO3 |
分析 根据加入的盐酸质量和选项中所给的固体物质的质量,结合化学方程式分析固体物质是否过量,然后分析生成气体的质量是否相等.
解答 解:A、2.4g的镁与酸反应会生成0.2g的氢气,钙会与水反应生成氢氧化钙和氢气,但是2.4g的钙会与2.4的镁生成的氢气质量不相等,所以反应停止后天平一定不平衡,故A正确;
B、5.6g的铁与盐酸反应会生成0.2g氢气,5.6g的锌生成的氢气小于0.2g,5.6g的镁与100g溶质质量分数为7.3%的稀盐酸等于0.2g,所以反应停止后天平可能不平衡,故B错误;
C、10g碳酸钙和盐酸反应会生成4.4g二氧化碳,溶液质量增大5.6g,5.6g氧化钙反应后溶液质量增大5.6g,所以反应停止后天平一定平衡,故C错误;
D、8.4gMg(OH)2与盐酸反应烧杯会增大8.4g,8.4gMg2CO3会生成,烧杯增加的质量小于8.4g,所以反应停止后天平一定不平衡,故D正确.
故选:AD.
点评 加入物质充分反应后,天平一端增加的质量=加入固体质量-放出气体的质量,只有加入物质与放出气体质量均相等时,天平才能保持平衡.由于运算量比较大,所以对于有关化学方程式的计算是否熟练是解题的关键.

练习册系列答案
相关题目
7.2015年10月5日,瑞典诺贝尔医学奖评委会宣布,我国著名药学家屠哟哟获得了诺贝尔生理学或医学奖,表彰她在研究青嵩素上获得重大突破,青嵩素(化学式为C15H22O5) 是一种用于治疗疟疾的药物.下列关于青嵩素的说法中正硧的是( )
| A. | 青嵩素是一种氧化物 | |
| B. | 青嵩素中氧元素的质量分数为11.9% | |
| C. | 青嵩素中C、H、O三种元素的质量比为90:11:40 | |
| D. | 青嵩素是由15个碳原子、22个氢原子和5个氧原子构成 |
8.下列属于复合肥的是( )
| A. | NH4NO3 | B. | NH4H2PO4 | C. | KCl | D. | Ca (H2PO4)2 |
5.下列有关处理燃烧与灭火的方法正确的是( )
| A. | 档案资料着火,可用液态二氧化碳灭火器扑灭 | |
| B. | 室内物品着火,应先打开门窗通风 | |
| C. | 降低可燃物的着火点,达到灭火的目的 | |
| D. | 高层建筑内发生火灾时,人们应该乘电梯快速下楼 |
6.下列有关能源资源叙述中正确的是( )
| A. | 新能源的开发和利用很重要,所以我们应该大力开发水能、电能、核能等新能源 | |
| B. | 我国的金属矿藏比较丰富,其中金、银、铜等金属都以单质的形式存在 | |
| C. | 作为高能燃料,液氢已应用于航天等领域 | |
| D. | 我们周围的空气可以用于化肥,炼钢,石油加工等,但不能用于发电 |
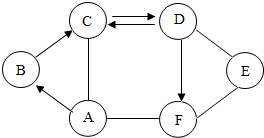 如图中:A、B、C、D、E、F是初中化学中的常见物质,其中B是一种气体单质,D是大理石的主要成分,“---”表示两端的物质能发生反应,“→”表示一种物质可转化为另一种物质,请回答:
如图中:A、B、C、D、E、F是初中化学中的常见物质,其中B是一种气体单质,D是大理石的主要成分,“---”表示两端的物质能发生反应,“→”表示一种物质可转化为另一种物质,请回答:
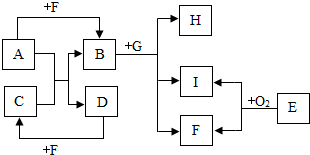 如图中所涉及到的物质均为初中化学常见物质,它们之间的转化关系如图所示(图中反应条件均已略去).其中A、D都是碱,A溶液与C溶液能发生复分解反应;E是天然气的主要成分.请回答下列问题:
如图中所涉及到的物质均为初中化学常见物质,它们之间的转化关系如图所示(图中反应条件均已略去).其中A、D都是碱,A溶液与C溶液能发生复分解反应;E是天然气的主要成分.请回答下列问题: