题目内容
8.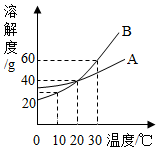 如图所示为A、B两种固体物质的溶解度曲线,根据溶解度曲线判断下列说法正确的是( )
如图所示为A、B两种固体物质的溶解度曲线,根据溶解度曲线判断下列说法正确的是( )| A. | 20℃时,A的饱和溶液溶质质量分数是40% | |
| B. | 100克30℃时B饱和溶液降温到20℃能析出20克B晶体(B不含结晶水) | |
| C. | 30℃时,若要配置100克B饱和溶液,需要溶质37.5克 | |
| D. | 20℃时饱和A溶液升温到30℃时溶液变成不饱和,溶质质量分数变大 |
分析 A、据20℃时A的溶解度分析解答;
B、据30℃时A的溶解度分析解答;
C、据该温度下B的溶解度及溶质的质量分数分析解答;
D、A的溶解度随温度升高而增大分析解答.
解答 解:A、20℃时A的溶解度是40g,饱和时质量分数的计算式$\frac{溶解度}{溶解度+100g}$×100%,则其饱和溶液中溶质的质量分数是:$\frac{40g}{140g}$×100%<40%,故错误;
B、30℃时B的溶解度是60g,即100g水中最多溶解60g的B,所以100克30℃时B饱和溶液所含溶质的质量小于60g,降温到20℃时其溶解度变为分0g,则能析出晶体的质量一定小于20克,故错误;
C、30℃时B的溶解度是60g,则160g饱和溶液中含有60g的B,则配置100克B饱和溶液,需要溶质的质量是:$\frac{60g}{160g}$×100g=37.5克,正确;
D、20℃时饱和A溶液升温到30℃时溶液变成不饱和,溶液中溶质、溶剂的质量不变,则溶质质量分数不变,故错误;
故选C.
点评 了解溶解度、溶解度曲线的意义并会应用,以及饱和溶液中溶质的质量分数的计算式,才能正确分析解答.

练习册系列答案
相关题目
18.下列关于金属的说法正确的是( )
| A. | 铁是地壳中含量最高的金属元素 | |
| B. | 铜的性能优良,是很纯的铁 | |
| C. | 铁制品生锈产生的铁锈是一种疏松多孔的物质,它的主要成分是Fe3O4 | |
| D. | 波尔多液不可以在铁制容器中配制 |
19.果糖大量存在于水果中,其化学式为C6H12O6,下列说法不正确的是( )
| A. | 1个果糖分子中碳、氢、氧的原子个数比为:1:2:1 | |
| B. | 果糖中碳、氢、氧元素质量比为:1:2:1 | |
| C. | 果糖由碳、氢、氧元素组成 | |
| D. | 1个果糖分子中含有24个原子 |
3.下列有关实验操作的“先”与“后”的说法中不正确的是( )
| A. | 制取气体时,先检查装置的气密性,后装药品 | |
| B. | 加热高锰酸钾并用排水法收集氧气实验结束时,先熄灭酒精灯,后移出导管 | |
| C. | 点燃可燃性气体前,先检验气体的纯度,后点燃 | |
| D. | 加热试管时,先使试管底部均匀受热,后用酒精灯的外焰固定加热 |
13.通过如图所示实验可以得出的结论中不合理的是( )
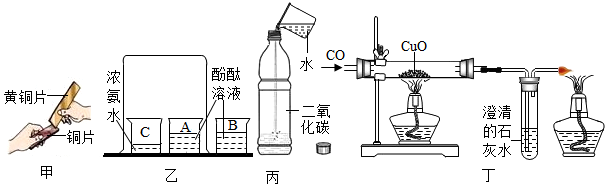

| A. | 甲实验中黄铜片能在铜片上刻画出痕迹并不能说明黄铜的密度比铜片大 | |
| B. | 乙实验既可以说明分子在不停地运动着,又可以说明氨水显碱性 | |
| C. | 丙实验既可以说明二氧化碳易溶于水,又可以说明二氧化碳具有酸性 | |
| D. | 丁实验既可以说明一氧化碳具有还原性,又可以说明一氧化碳具有可燃性 |
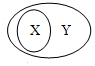 14、中的X、Y的关系为Y包含X,下列选项中符合图中关系的是( )
14、中的X、Y的关系为Y包含X,下列选项中符合图中关系的是( )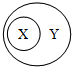 下列选项符合图示从属关系的是( )
下列选项符合图示从属关系的是( )