题目内容
根据如图实验装置图,回答问题:
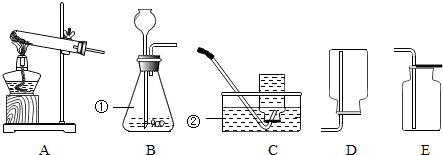
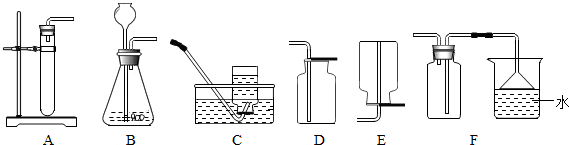
(1)写出标有序号的仪器名称:① ,② .
(2)在实验室中用高锰酸钾制取氧气时,发生反应的化学方程式为 ,应选择的发生装置为 (填装置的字母代号,下同),该装置还缺少的实验用品是 .
(3)二氧化硫是易溶于不、密度比空气大的气体,实验室常用亚硫酸钠固体和稀硫酸在常温下反应制取二氧化硫,反应的化学方程式为 ,应选用 装置进行收集,为防止多余的二氧化硫污染空气,最好用 来吸收.

(1)写出标有序号的仪器名称:①
(2)在实验室中用高锰酸钾制取氧气时,发生反应的化学方程式为
(3)二氧化硫是易溶于不、密度比空气大的气体,实验室常用亚硫酸钠固体和稀硫酸在常温下反应制取二氧化硫,反应的化学方程式为
考点:常用气体的发生装置和收集装置与选取方法,实验室制取氧气的反应原理,碱的化学性质,书写化学方程式、文字表达式、电离方程式
专题:常见气体的实验室制法、检验、干燥与净化
分析:(1)熟练掌握化学常见仪器的名称和用途;
(2)根据反应物的状态和反应条件选择发生装置;高锰酸钾加热分解产生锰酸钾、二氧化锰和氧气;根据
(3)亚硫酸钠固体和稀硫酸在常温下反应制取二氧化硫;根据二氧化硫的密度和溶解性选择收集装置,二氧化硫有毒,为防止多余的二氧化硫污染空气,最好用NaOH溶液来吸收.
(2)根据反应物的状态和反应条件选择发生装置;高锰酸钾加热分解产生锰酸钾、二氧化锰和氧气;根据
(3)亚硫酸钠固体和稀硫酸在常温下反应制取二氧化硫;根据二氧化硫的密度和溶解性选择收集装置,二氧化硫有毒,为防止多余的二氧化硫污染空气,最好用NaOH溶液来吸收.
解答:解:
(1)①是锥形瓶;②是水槽;
(2)高锰酸钾加热分解产生锰酸钾、二氧化锰和氧气,故发生装置的特点是固体加热型的A装置;反应的方程式为:2KMnO4
K2MnO4+MnO2+O2↑;为防止高锰酸钾随气流进入导气管,试管口应放棉花;
(3)亚硫酸钠固体和稀硫酸在常温下反应制取二氧化硫,反应的化学方程式为Na2SO3+H2SO4═Na2SO4+SO2↑+H2O;二氧化硫是易溶于不、密度比空气大的气体,故选用E收集;二氧化硫有毒,为防止多余的二氧化硫污染空气,最好用NaOH溶液来吸收.
答案:
(1)①锥形瓶 ②水槽
(2)2KMnO4
K2MnO4+MnO2+O2↑ A 棉花
(3)Na2SO3+H2SO4═Na2SO4+SO2↑+H2O E NaOH溶液
(1)①是锥形瓶;②是水槽;
(2)高锰酸钾加热分解产生锰酸钾、二氧化锰和氧气,故发生装置的特点是固体加热型的A装置;反应的方程式为:2KMnO4
| ||
(3)亚硫酸钠固体和稀硫酸在常温下反应制取二氧化硫,反应的化学方程式为Na2SO3+H2SO4═Na2SO4+SO2↑+H2O;二氧化硫是易溶于不、密度比空气大的气体,故选用E收集;二氧化硫有毒,为防止多余的二氧化硫污染空气,最好用NaOH溶液来吸收.
答案:
(1)①锥形瓶 ②水槽
(2)2KMnO4
| ||
(3)Na2SO3+H2SO4═Na2SO4+SO2↑+H2O E NaOH溶液
点评:本题考查了常见气体的制取和收集及根据化学方程式的计算,在计算中关键是根据坐标分析已知量进行相关解题.

练习册系列答案
相关题目
善于用化学的眼光看世界,能够提高我们的科学素养,你认为下列变化事实和相应的解释不一致的是( )
| A、牛奶变酸是化学变化 |
| B、缉毒犬能嗅出毒品,是因为分子在不断运动 |
| C、能将25cm3的石油气装入0.024cm3的钢瓶中,是因为分子之间有间隔 |
| D、温度计中的水银(汞)柱遇热上升,是国为原子本身的大小发生了改变 |

 铁锅都是生活中常用的饮具,如图是铁锅的示意图.
铁锅都是生活中常用的饮具,如图是铁锅的示意图.