题目内容
20.将3g二氧化锰加到100g过氧化氢溶液中,完全反应后称得剩余物质的总质量为99.8g.求:(1)生成氧气的质量;(2)求过氧化氢溶液中过氧化氢的质量.
分析 反应前各物质的质量总和应为过氧化氢溶液和二氧化锰的质量和.反应中仅有氧气放出,再利用质量守恒定律即可求得氧气的量.最后利用所求氧气的质量求出过氧化氢溶液中溶质过氧化氢的质量.
解答 解:(1)反应前各物质的质量总和=100g+3g=103g,反应后剩余物质的总质量为99.8g,所以反应放出氧气的质量=103g-99.8g=3.2g;
(2)设:过氧化氢的物质的质量为x
2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
68 32
x 3.2g
$\frac{68}{x}$=$\frac{32}{3.2g}$
x=6.8g
故答案为:(1)3.2;
(2)所取溶液中过氧化氢的质量为6.8g.
点评 本题为最基本的根据化学方程式的计算题,解答本题的关键是根据质量守恒定律求出氧气的质量.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
5. 要使如图装置中的小气球鼓起来,则使用的固体和液体可以是( )
要使如图装置中的小气球鼓起来,则使用的固体和液体可以是( )
①氢氧化钠固体和水 ②镁和稀硫酸 ③二氧化锰和过氧化氢溶液
④硝酸铵和水.
 要使如图装置中的小气球鼓起来,则使用的固体和液体可以是( )
要使如图装置中的小气球鼓起来,则使用的固体和液体可以是( )①氢氧化钠固体和水 ②镁和稀硫酸 ③二氧化锰和过氧化氢溶液
④硝酸铵和水.
| A. | ①②③④ | B. | ①②③ | C. | ①②④ | D. | ②③④ |

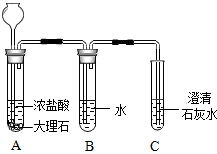 已知盐酸是HCI气体溶于水所形成的溶液,在实验室制取二氧化碳并检验其性质的实验中,如果用浓盐酸代替稀盐酸,并将产生的气体通入澄清的石灰水,往往看不到溶液变浑浊的现象,现有一同学用下列装置进行实验,却看到了澄清石灰水变浑浊的现象.
已知盐酸是HCI气体溶于水所形成的溶液,在实验室制取二氧化碳并检验其性质的实验中,如果用浓盐酸代替稀盐酸,并将产生的气体通入澄清的石灰水,往往看不到溶液变浑浊的现象,现有一同学用下列装置进行实验,却看到了澄清石灰水变浑浊的现象.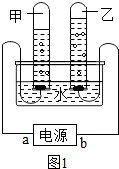 水-生命之源
水-生命之源