题目内容
 某初三化学兴趣小组同学,在对氧气性质进行研究时,设计了如下实验:
某初三化学兴趣小组同学,在对氧气性质进行研究时,设计了如下实验:①小李同学取一段铁丝窗网上的细铁丝,在自己收集到的氧气中做“铁丝在氧气中燃烧”的实验,结果没有观察到“火星四射”的现象.造成此实验失败的原因可能是
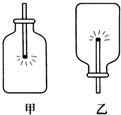
②小王同学将用排水法收集满氧气的两个集气瓶按如图所示放置,并分别同时迅速插入一根带火星的木条,发现木条均复燃,且甲中燃烧比乙中更旺,该实验说明氧气具有的性质是
③在实验探究的过程中组长有同学提出:能使带火星的木条复燃所需氧气的最低体积分数是多少?
小组同学查阅资料得出的结论是:能使带火星木条复燃所需氧气的最低体积分数应在30%~50%之间.
这时小陆同学又提出:能否使实验数据更加具体和准确些?小组同学又略经讨论,进行实验,得到的现象如图所示:
| 1号瓶 (收集34%的氧气) | 2号瓶 (收集35%的氧气) | 3号瓶 (收集36%的氧气) | 4号瓶 (收集37%的氧气) |
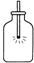 不复燃 不复燃 |  不复燃,但很亮 不复燃,但很亮 |  很亮,复燃 很亮,复燃 |  立即复燃 立即复燃 |
考点:探究氧气的性质,反应类型的判定,书写化学方程式、文字表达式、电离方程式
专题:科学探究
分析:(1)做铁丝在氧气中燃烧这个实验时.要注意:铁丝不能太粗;铁丝不能生锈;铁丝要在纯氧中燃烧;铁丝的下端要用火柴引燃;集气瓶的底部要放水或铺沙子等.
(2)氧气的验证:能使带火星木条复燃.密度大于空气的气体,存放时集气瓶应正放,减少气体的逸散.
(3)分析表格可发现收集的氧气占容积的体积分数最低为36%时木条就可复燃,根据空气中原有的氧气和收集到的氧气,就可算出氧气的分数.
(2)氧气的验证:能使带火星木条复燃.密度大于空气的气体,存放时集气瓶应正放,减少气体的逸散.
(3)分析表格可发现收集的氧气占容积的体积分数最低为36%时木条就可复燃,根据空气中原有的氧气和收集到的氧气,就可算出氧气的分数.
解答:解:(1)做“铁丝在氧气中燃烧”的实验.没有观察到“火星四射”的现象,实验失败的可能原因是:铁丝已经生锈;收集的氧气不纯;温度没有达到铁的着火点等.防止溅落的熔化物炸裂瓶底;集气瓶的底部要放水或铺沙子.
铁在氧气中燃烧生成了四氧化三铁,反应的文字表达式是:铁+氧气
四氧化三铁.该反应由两种物质生成了一种物质,属于化合反应.
故答案为:铁丝生锈;铁+氧气
四氧化三铁;化合反应.
(2)氧气的密度比空气的密度大,收集后要用瓶口向上.如果瓶口向下的话,则收集的氧气可能会逸出.甲图中瓶口向上,而乙图瓶口向下,故乙图中的氧气含量少.氧气又能使带火星的木条复燃.因而在甲中燃烧比在乙更旺.故答案为:氧气的密度比空气的密度大;氧气能助燃(能支持燃烧).
(3)因该瓶中还有体积为64%的空气,空气中也有氧气,所以这位同学的观点不正确.观察实验记录,收集的氧气占容积的体积分数最低为36%,带火星的木条复燃,此时空气还占64%,所以空气中有氧气的量为:64%×21%≈13%,所以此时瓶内共有氧气的分数为:13%+36%=49%.
故答案为:该瓶中还有体积为64%的空气,空气中也有氧气;49%;
铁在氧气中燃烧生成了四氧化三铁,反应的文字表达式是:铁+氧气
| 点燃 |
故答案为:铁丝生锈;铁+氧气
| 点燃 |
(2)氧气的密度比空气的密度大,收集后要用瓶口向上.如果瓶口向下的话,则收集的氧气可能会逸出.甲图中瓶口向上,而乙图瓶口向下,故乙图中的氧气含量少.氧气又能使带火星的木条复燃.因而在甲中燃烧比在乙更旺.故答案为:氧气的密度比空气的密度大;氧气能助燃(能支持燃烧).
(3)因该瓶中还有体积为64%的空气,空气中也有氧气,所以这位同学的观点不正确.观察实验记录,收集的氧气占容积的体积分数最低为36%,带火星的木条复燃,此时空气还占64%,所以空气中有氧气的量为:64%×21%≈13%,所以此时瓶内共有氧气的分数为:13%+36%=49%.
故答案为:该瓶中还有体积为64%的空气,空气中也有氧气;49%;
点评:做铁丝在氧气中燃烧这个实验时,一定要在集气瓶的底部放少量的水或沙子,以防止热的生成物落到瓶底,使瓶底炸裂.设计实验时,要明确实验的目的,要注意控制一些变量,从而可减少实验的次数,减少实验的过程.

练习册系列答案
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案
相关题目
为完成下列四个实验,编号处所指物质的选用正确的是( )
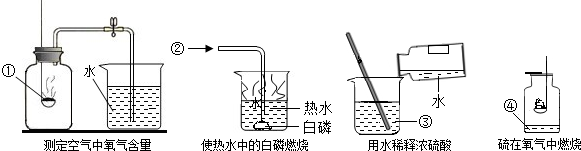

| A、①木炭 | B、②氮气 |
| C、③浓硫酸 | D、④水 |
如图是实验室制备、收集、验满、验证性质的操作,其中不正确的是( )
A、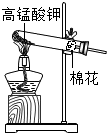 |
B、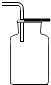 |
C、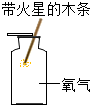 |
D、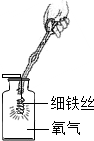 |
关于蜡烛燃烧实验现象描述错误的是( )
| A、放出大量的热 |
| B、发出黄色的火焰 |
| C、生成二氧化碳和水 |
| D、火焰分成三层 |
下列选项所用试剂无法鉴别组内物质的是( )
| A、用熟石灰鉴别氯化铵﹑氯化钾 |
| B、用稀盐酸鉴别碳酸钠粉末﹑碳酸钾粉末 |
| C、用硫酸铜溶液鉴别氢氧化钠﹑硝酸钠溶液 |
| D、用硫酸铜溶液鉴别氢氧化钠﹑硝酸钠溶液 |
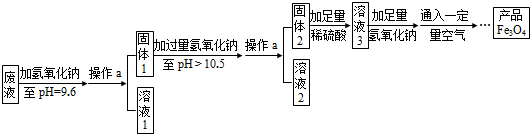
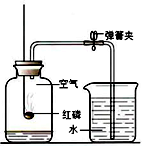 某同学用如图装置测定空气中氧气的体积分数.请你填写有关空格.
某同学用如图装置测定空气中氧气的体积分数.请你填写有关空格.