题目内容
11.硫化氢(H2S) 是一种没有颜色,具有臭鸡蛋气味的有毒气体,其密度比空气大,且能溶于水形成氢硫酸,在空气中点燃硫化氢气体有SO2和水生成.实验室通常用块状固体硫化亚铁(FeS),与稀硫酸混合,在常温下发生复分解反应,制得硫化氢气体,试回答: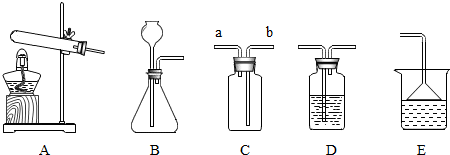
(1)具有臭鸡蛋气味,这属H2S的物理性质.(物理或化学)?
(2)写出制取硫化氢气体的化学方程式FeS+H2SO4=FeSO4+H2S↑.
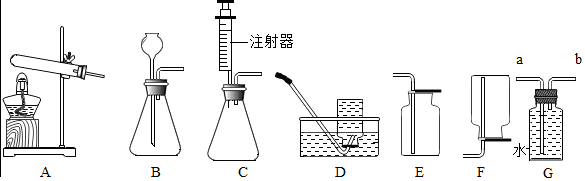
(3)根据装置图回答下列问题:?
①制取H2S气体的发生装置可选用B?
②若用C装置收集H2S气体,进气口应为b?
③为了验证硫化氢的水溶液呈酸性,可将气体通入装置D.D中所盛的试剂应该是紫色石蕊试液,反应现象为紫色变红色
④做上述实验时,为了防止多余的H2S气体逸出污染环境,可将其通入装置E吸收.E中试剂应为氢氧化钠溶液.?
分析 具有臭鸡蛋气味,这属H2S的物理性质;制取装置包括加热和不需加热两种,实验室通常用块状固体硫化亚铁(FeS),与稀硫酸混合,在常温下发生复分解反应,制得硫化氢气体,因此不需要加热;若用C装置收集H2S气体,进气口应长管,因为硫化氢气体的密度比空气大;为了验证硫化氢的水溶液呈酸性,可将气体通入装置D,D中所盛的试剂应该是紫色石蕊试液,现象是紫色变红色;为了防止多余的H2S气体逸出污染环境,可将其通入氢氧化钠溶液中吸收.
解答 解:(1)具有臭鸡蛋气味,这属H2S的物理性质,故答案为:物理;
(2)固体硫化亚铁(FeS),与稀硫酸混合反应生成硫酸亚铁和硫化氢,配平即可;故答案为:FeS+H2SO4=FeSO4+H2S↑;
(3)实验室通常用块状固体硫化亚铁(FeS),与稀硫酸混合,在常温下发生复分解反应,制得硫化氢气体,因此不需要加热;若用C装置收集H2S气体,进气口应长管,因为硫化氢气体的密度比空气大;为了验证硫化氢的水溶液呈酸性,可将气体通入装置D,D中所盛的试剂应该是紫色石蕊试液,现象是紫色变红色;为了防止多余的H2S气体逸出污染环境,可将其通入氢氧化钠溶液中吸收;故答案为:①B;②b;③紫色石蕊试液;紫色变红色;④氢氧化钠溶液;
点评 本考点主要考查了硫化氢的性质、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和气体的性质等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
1.如表列出了 20℃时NaCl溶解实验的一组数据.
以上实验组中,得到的溶液属于饱和溶液的是③④(填序号),由如表的数据可知在20℃时,NaCl溶解度为36g.
| 实验序号 | 水的质量/g | 所加NaCl的质量/g | 所得溶液的质量/g |
| ① | 100 | 20 | 120 |
| ② | 100 | 30 | 130 |
| ③ | 100 | 36 | 136 |
| ④ | 100 | 40 | 136 |
2.构建和谐社会,建设社会主义新农村的目标之一是让农民饮用清洁的自来水.自来水消毒过程中常会发生甲、乙化学反应,其反应的微观过程可用如图表示:下列说法正确的是( )
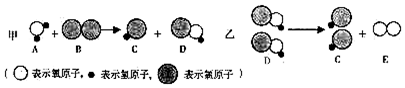

| A. | 物质A的化学式是H2O | B. | 物质C的水溶液pH大于7 | ||
| C. | 甲是复分解反应 | D. | E物质是化合物 |
6.下列现象与物质状态变化的联系正确的是( )
| A. | 冬天从嘴里呼出的“白汽”:汽化 | |
| B. | 电流过大时,电路中保险丝熔断:熔化 | |
| C. | 湿衣服凉干:液化 | |
| D. | 硫酸铜溶液中加入氢氧化钠溶液产生蓝色沉淀:凝固 |
20.下列实验操作能达到实验目的是( )
| 选项 | 实验目的 | 实验操作 |
| A | 鉴别空气、氧气和氮气 | 燃着的木条 |
| B | 除去CuSO4溶液中的少量FeSO4 | 加入足量铜粉 |
| C | 鉴别澄清石灰水和NaOH溶液 | 加入稀盐酸 |
| D | 鉴别氯化钠溶液和稀盐酸 | 酚酞溶液 |
| A. | A | B. | B | C. | C | D. | D |
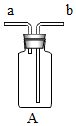 利用如图该瓶的装置有多个用途:
利用如图该瓶的装置有多个用途: