题目内容
20.在煤中加入适量的生石灰(CaO)制成供居民采暖用的“环保煤”,以减少二氧化硫的排放,减弱二氧化硫对空气的污染.燃烧时生石灰吸收二氧化硫的化学方程式为:2CaO+2SO2+O2$\frac{\underline{\;高温\;}}{\;}$2CaSO4,请计算.(1)二氧化硫中硫、氧元素的质量比为1:1.
(2)若煤厂一次共加入含氧化钙80%的生石灰1400t,则理论上最多可吸收二氧化硫多少吨?
分析 (1)根据化合物中各元素的质量比,即为化学式中各原子的相对原子质量和的比解答;
(2)根据化学方程式的计算,有一种反应物可以求出另一种物质的质量.
解答 解:
(1)二氧化硫(SO2)中硫元素与氧元素的质量比为:32:(16×2)=1:1.
(2)设理论上最多可吸收SO2的质量为x.
氧化钙的质量=1400t×80%=1120t
2CaO+2SO2+O2$\frac{\underline{\;高温\;}}{\;}$ 2CaSO4
112 128
1120t x
$\frac{112}{1120t}=\frac{128}{x}$
x=1280t
答案:
(1)1:1
(2)理论上最多可吸收SO21280t.
点评 本题主要考查化学式的意义、根据化学式确定组成物质元素之间的质量关系.

练习册系列答案
相关题目
10.下列实验现象的描述不正确的是( )
| A. | 把二氧化碳通入石蕊溶液,溶液变红 | |
| B. | 硫在空气中燃烧生成二氧化硫 | |
| C. | 硝酸铵固体溶于水时吸收热量 | |
| D. | 打开浓盐酸的瓶盖,瓶口出现大量白雾 |
11.下列图象有关量的变化趋势不能正确反映其对应操作的是( )
| A. |  向一定量的水中加入生石灰 | |
| B. | 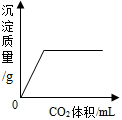 在一定量的CaCl2溶液中通入CO2气体 | |
| C. |  向NaOH和Na2CO3的混合溶液中逐滴加入稀盐酸 | |
| D. | 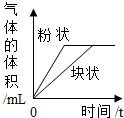 等质量CaCO3分别与等体积等质量分数的稀盐酸(足量)反应 |
8.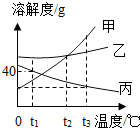 如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是( )
如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是( )
 如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是( )
如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法错误的是( )| A. | t2℃时,甲、乙两种物质的饱和溶液中溶质质量相等 | |
| B. | 甲和乙的溶解度都随温度的升高而增大 | |
| C. | 分别将t3℃时甲、乙、丙的饱和溶液降温至t1℃,则所得的三种溶液中溶质的质量分数大小关系是乙>甲>丙 | |
| D. | t1℃时,甲、丙的饱和溶液中溶质的质量分数为40% |
5.如表是NaCl和NH4C1在不同温度时的溶解度.下列说法不正确的是( )
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 | 38.4 | 39.0 | 39.8 |
| NH4C1 | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | 60.2 | 65.6 | 71.3 | 77.3 |
| A. | NH4C1的溶解度受温度影响比NaCl大 | |
| B. | 在10-20℃时,两种物质可配制相同溶质质量分数的饱和溶液 | |
| C. | 20℃时,100g饱和 NaCl溶液中含有36.0gNaCl | |
| D. | 若 NH4C1固体中含有少量NaCl,可采用降温结晶的方法提纯NH4Cl |
9.甲同学为了区别氢氧化钠和氢氧化钙溶液,设计了下图所示的四组实验方案.
(1)其中能达到实验目的是C、D.
(2)在C组实验中发生的化学方程式为Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
(3)实验结束后,甲同学将A、C组四支试管中的溶液倒入同一容器中,看到溶液变浑浊,该现象说明有CaCO3物质生成(填化学式),滴入酚酞后溶液呈红色.
(4)滴入酚酞后溶液呈红色,说明溶液呈碱性.使溶液呈碱性的物质是什么呢?甲同学进一步推测:溶液中呈碱性的物质可能是碳酸钠、氢氧化钙和NaOH三种物质中的一种,或是三种物质两两混合组成的混合物.
(5)为了验证推测,甲同学查阅资料,获悉氯化钡溶液呈中性,并设计如下实验加以验证.请根据要求完成下列空白:
(6)乙同学认为甲同学第②步验证的结论不严密,原因是氢氧化钠溶液也显碱性,还可能是氢氧化钠或氢氧化钠和氢氧化钙的混合物.

(1)其中能达到实验目的是C、D.
(2)在C组实验中发生的化学方程式为Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
(3)实验结束后,甲同学将A、C组四支试管中的溶液倒入同一容器中,看到溶液变浑浊,该现象说明有CaCO3物质生成(填化学式),滴入酚酞后溶液呈红色.
(4)滴入酚酞后溶液呈红色,说明溶液呈碱性.使溶液呈碱性的物质是什么呢?甲同学进一步推测:溶液中呈碱性的物质可能是碳酸钠、氢氧化钙和NaOH三种物质中的一种,或是三种物质两两混合组成的混合物.
(5)为了验证推测,甲同学查阅资料,获悉氯化钡溶液呈中性,并设计如下实验加以验证.请根据要求完成下列空白:
| 实验内容 | 预测现象 | 结论 |
| 取少量容器中的上层溶液于试管中,加入过量的氯化钡溶液,静置 | ①若有白色沉淀,溶液呈无色 | 物质是碳酸钠 |
| ②若无沉淀生成,溶液呈红色 | 物质是氢氧化钙 | |
| ③若有白色沉淀,溶液呈红色 | 物质是碳酸钠和氢氧化钠的混合物 |
 某化肥说明书的一部分如图.
某化肥说明书的一部分如图.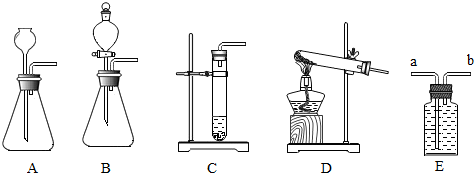
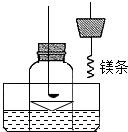 某科学兴趣小组查阅资料得知镁可在氮气中燃烧生成Mg3N2,设计了如下方案进行验证.
某科学兴趣小组查阅资料得知镁可在氮气中燃烧生成Mg3N2,设计了如下方案进行验证.