题目内容
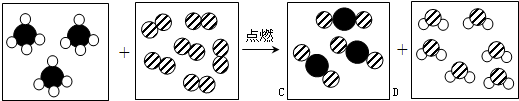
 如图是甲、乙两种固体物质的溶解度曲线.
如图是甲、乙两种固体物质的溶解度曲线.(1)t1℃时甲、乙两种物质的溶解度大小关系为:甲
(2)将等质量的甲、乙两种固体物质分别制成t3℃饱和溶液,所制得溶液质量的大小关系为:甲
(3)将等质量的t2℃甲、乙两种饱和溶液,升高温度到t3℃所得溶液的溶质质量分数的大小关系为:甲
(4)用t3℃时甲的饱和溶液配制5%的甲溶液,需要用到的仪器有烧杯、玻璃棒还需要
考点:固体溶解度曲线及其作用,一定溶质质量分数的溶液的配制,溶质的质量分数、溶解性和溶解度的关系
专题:溶液、浊液与溶解度
分析:(1)根据某一温度时物质溶解度的比较方法考虑;
(2)根据t3℃甲和乙的溶解度考虑;
(3)根据升温后溶解度的变化考虑;
(4)根据配制溶液用到的仪器考虑.
(2)根据t3℃甲和乙的溶解度考虑;
(3)根据升温后溶解度的变化考虑;
(4)根据配制溶液用到的仪器考虑.
解答:解:(1)从t1℃向上做垂线,与曲线的交点在上面的溶解度就大,所以t1℃时它们的溶解度大小顺序是甲<乙;
(2)t3℃甲的溶解度大于乙的溶解度,所以溶解等质量的甲和乙物质,甲物质需要的水质量少,乙物质需要的水质量多,所以将等质量的甲、乙两种固体物质分别制成t3℃饱和溶液,所制得溶液质量甲<乙;
(3)饱和溶液溶质质量分数=
×100%,所以溶解度大溶质质量分数就大,t2℃甲、乙两种物质的溶解度相等,所以该温度下饱和溶液的溶质质量分数相等,升温后溶解度增大,溶液由饱和变为不饱和,溶质质量分数不变,所以还是相等;
(4)配制溶液时需要先计算,再进行称量,用到量筒和胶头滴管,配制溶液要在烧杯中进行,用玻璃棒搅拌,
故答案为:(1)<;(2)<;(3)=;(4)胶头滴管;量筒.
(2)t3℃甲的溶解度大于乙的溶解度,所以溶解等质量的甲和乙物质,甲物质需要的水质量少,乙物质需要的水质量多,所以将等质量的甲、乙两种固体物质分别制成t3℃饱和溶液,所制得溶液质量甲<乙;
(3)饱和溶液溶质质量分数=
| 溶解度 |
| 100g+溶解度 |
(4)配制溶液时需要先计算,再进行称量,用到量筒和胶头滴管,配制溶液要在烧杯中进行,用玻璃棒搅拌,
故答案为:(1)<;(2)<;(3)=;(4)胶头滴管;量筒.
点评:解答本题关键是要知道溶解度大小的比较方法,饱和溶液溶质质量分数的计算公式=
×100%.
| 溶解度 |
| 100g+溶解度 |

练习册系列答案
相关题目
下列各组金属中,按金属活动性由弱到强顺序排列的是( )
| A、Zn、Na、Hg |
| B、Mg、Na、Cu |
| C、Fe、Zn、Al |
| D、Mg、Hg、Cu |
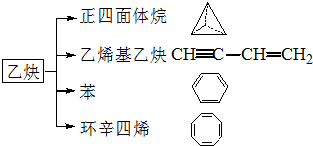
 表示碳原子,
表示碳原子, 表示氧原子,
表示氧原子, 表示氢原子.
表示氢原子.