题目内容
12.利用纯净、干燥的氢气还原灼热的氧化铜来测定水的组成.实验装置由A、B、C、D组成(氢气发生装置省略,未画出).回答下列问题: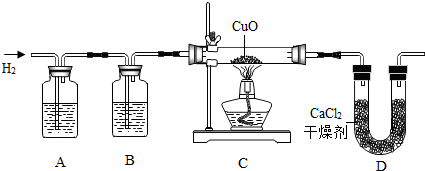
(1)如果某学生用锌和较浓的盐酸制取氢气,他用装置A、B是为了得到纯净、干燥的氢气,在装置A中通常盛放氢氧化钠溶液,为了除去氯化氢气体 _;在装置B中应盛放的试剂是浓硫酸,为了除去水蒸气.
(2)若实验前后,称量结果如下,装氧化铜的玻璃管的质量减少了6.4g,装氯化钙的U型管的质量增加了7.2g.根据上述实验数据写出水中氢、氧两种元素质量比的原始计算式(7.2g-6.4g):6.4g.
(3)为了减少误差,实验结束后冷却的过程中需要注意的问题是持续通入氢气直至玻璃管冷却至室温.
分析 (1)浓盐酸易挥发,产生的氢气中含有氯化氢气体和水蒸气;
氢氧化钠溶液能够吸收氯化氢气体,并且能和氯化氢气体反应生成氯化钠和水;
浓硫酸具有吸水性,可以用作氢气、氧气、二氧化碳等气体的干燥剂;
(2)装氧化铜的玻璃管的质量减少了6.4g,说明说明生成的水中含有6.4g氧元素,装氯化钙的U型管的质量增加了7.2g,说明反应生成了7.2g水;
(3)加热条件下,铜能被空气中的氧气氧化成氧化铜.
解答 解:(1)用锌和较浓的盐酸制取氢气时,用装置A、B是为了得到纯净、干燥的氢气,在装置A中通常盛放氢氧化钠溶液,为了除去氯化氢气体;
在装置B中应盛放的试剂是浓硫酸,为了除去水蒸气.
故填:氢氧化钠;氯化氢气体;浓硫酸;水蒸气.
(2)装氧化铜的玻璃管的质量减少了6.4g,说明生成的水中含有6.4g氧元素,装氯化钙的U型管的质量增加了7.2g,说明反应生成了7.2g水;
根据上述实验数据,水中氢、氧两种元素质量比的原始计算式为:(7.2g-6.4g):6.4g.
故填:(7.2g-6.4g):6.4g.
(3)为了减少误差,实验结束后冷却的过程中需要持续通入氢气直至玻璃管冷却至室温,这样能够防止生成的铜被氧气.
故填:持续通入氢气直至玻璃管冷却至室温.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
3.3.0克某物质完全燃烧,生成4.4克二氧化碳和1.8克水,下列有关判断正确的是( )
| A. | 该物质一定含有碳、氢元素,可能含有氧元素 | |
| B. | 该物质一定不含氧元素 | |
| C. | 该物质中碳、氢元素的质量比为6:1 | |
| D. | 该物质分子中碳、氢原子个数比为1:1 |
7.下列离子能在PH=11的溶液中大量共存的是( )
| A. | K+ NO3- Na+ OH- | B. | CO32- Na+ Cl- Ca2+ | ||
| C. | H+ Ba2+ Cl- SO42- | D. | K+ NO3- SO42- Cu2+ |
4. 乙炔(C2H2)气体可由碳化钙固体(CaC2)与水反应生成,同时生成一种白色固体.
乙炔(C2H2)气体可由碳化钙固体(CaC2)与水反应生成,同时生成一种白色固体.
【査阅资料】Ca(OH)2与稀盐酸反应无气泡产生.
【提出问题】白色固体是什么物质?
【做出猜想】小明经过思考认为有以下两种可能:
猜想一:CaC03;猜想二:Ca(0H)2
【讨论交流】做出猜想一、二的理由是:化学反应前后原子的种类及数目不变.
【进行实验】设计实验验证白色固体不是碳酸钙.
【反思与结论】猜想二正确
①写出实验室制取乙炔的化学反应方程式CaC2+2H2O=Ca(OH)2+C2H2↑.
②乙炔和氧气反应能产生高温火焰,工人师傅常用氧炔焰切割或焊接金属,试写出该反应的化学方程式2C2H2+5O2$\frac{\underline{\;点燃\;}}{\;}$4CO2+2H2O,如图所示为氧炔焰切割机,乙炔与氧气按照2:5体积比混合点燃,焊接效果最好.
 乙炔(C2H2)气体可由碳化钙固体(CaC2)与水反应生成,同时生成一种白色固体.
乙炔(C2H2)气体可由碳化钙固体(CaC2)与水反应生成,同时生成一种白色固体.【査阅资料】Ca(OH)2与稀盐酸反应无气泡产生.
【提出问题】白色固体是什么物质?
【做出猜想】小明经过思考认为有以下两种可能:
猜想一:CaC03;猜想二:Ca(0H)2
【讨论交流】做出猜想一、二的理由是:化学反应前后原子的种类及数目不变.
【进行实验】设计实验验证白色固体不是碳酸钙.
| 实验步骤 | 实验现象 | 实验结论 |
| 白色固体不是碳酸钙 |
①写出实验室制取乙炔的化学反应方程式CaC2+2H2O=Ca(OH)2+C2H2↑.
②乙炔和氧气反应能产生高温火焰,工人师傅常用氧炔焰切割或焊接金属,试写出该反应的化学方程式2C2H2+5O2$\frac{\underline{\;点燃\;}}{\;}$4CO2+2H2O,如图所示为氧炔焰切割机,乙炔与氧气按照2:5体积比混合点燃,焊接效果最好.
 钙元素对人类生命和生活具有重要意义.
钙元素对人类生命和生活具有重要意义.