题目内容
3.根据要求填空(1)写出下列要求的化学符号
原子序号15P原子序号7N原子序号8O原子序号11Na
2个氧原子2O2个氧分子2O25个镁离子5Mg2+3个二氧化碳分子3CO2
(2)写出下列物质的名称
MgSO4硫酸镁 KCl氯化钾 P2O5五氧化二磷.
分析 (1)根据化学符号的书写方法分析:根据原子序号书写元素符号;原子直接用元素符号,多个微粒的表示是在微粒的符号前加上系数;离子用离子符号表示,多个微粒的表示是在微粒的符号前加上系数;分子用化学式表示,多个微粒的表示是在微粒的符号前加上系数;
(2)化合物化学式的读法:一般是从右向左读,读作“某化某”,有时还要把元素符号右下角的数字读出来,如SO2、P2O5等,据此进行分析解答.
解答 解:(1)15号元素是磷元素,符号为:P;7号元素为氮元素,符号为:N;8号元素为氧元素,符号为:O;11号元素为钠元素,符号为:Na;2个氧原子为表示为:2O;2个氧分子可表示为:2O2;5个镁离子可表示为:5Mg2+;3个二氧化碳分子可表示为:3CO2;
(2)MgSO4 读作硫酸镁; KCl读作氯化钾; P2O5读作五氧化二磷;
故填:硫酸镁;氯化钾;五氧化二磷;
点评 本题考查了粒子符号的书写及物质化学式的读法,这是学习化学的重点,中考必考知识,常以填空的形式出现,难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
14.下列图象与所述实验变化一致的是( )
| A. | 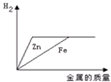 向等质量等浓度的稀盐酸中逐渐加入铁粉和锌粉,产生H2的质量随加入金属的变化关系 | |
| B. | 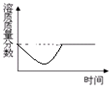 向一饱和澄清石灰水中加入一定量的氧化钙后,所得溶液的溶质质量分数随时间变化关系 | |
| C. | 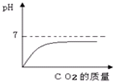 向一定量的水中持续通入二氧化碳气体,所得溶液的pH随通入二氧化碳质量的变化关系 | |
| D. | 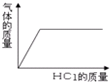 向部分变质的NaOH溶液中逐滴滴加稀盐酸,产生气体随加入稀盐酸质量的变化关 |
11.下列有关酸的性质说法正确的是( )
| A. | 浓硫酸与浓盐酸都具有吸水性 | |
| B. | 稀硫酸与稀盐酸都可以除铁锈 | |
| C. | 打开盛有浓硫酸与浓盐酸的试剂瓶瓶塞瓶口都有白雾 | |
| D. | 浓硫酸与浓硝酸长期放置液体的质量都会减少 |
15.鉴别空气、氧气、二氧化碳三瓶气体,最简单的方法是( )
| A. | 将气体分别通入蒸馏水中 | B. | 将气体分别通入澄清的石灰水中 | ||
| C. | 将燃着的木条分别伸入集气瓶中 | D. | 以上三种方法都可以 |
12.同学们一起探究铝、铁、铜三种金属的活动性,小刚同学设计了用铜丝、铁丝、铝丝和稀盐酸,只用一只试管,取一次盐酸的探究方案.请你和他们一起完善下表的探究方案并回答有关问题.
(1)【填表】
【结论】:金属活动性Al>Fe>Cu
(2)将铝丝插入前应进行的操作是用砂纸打磨;
(3)小华同学认为在小刚设计的方案中,只要补充一个实验,就可得出Al>Fe>H>Cu的结论.小华要补充的实验是把铜丝插入稀盐酸中;
(4)小强同学认为要得到Al>Fe>H>Cu的结论,不必做补充实验,只需将小明同学方案中插入金属的顺序调整即可,你认为调整后插入金属的顺序是Cu、Fe、Al.
(5)【归纳】比较金属活动性强弱的方法有①利用金属和酸的反应判断金属活动性②利用金属和盐溶液的反应判断金属活动性.
(1)【填表】
| 实验步骤 | 观察到的现象 |
| ①在试管中取少量盐酸,插入铁丝,充分作用. | |
| ②在①所得的溶液中,插入铜丝,充分作用. | 无明显现象 |
| ③在②所得的溶液中插入铝丝,充分作用. | 铝丝表面会覆盖一层黑色物质,溶液变为无色 |
(2)将铝丝插入前应进行的操作是用砂纸打磨;
(3)小华同学认为在小刚设计的方案中,只要补充一个实验,就可得出Al>Fe>H>Cu的结论.小华要补充的实验是把铜丝插入稀盐酸中;
(4)小强同学认为要得到Al>Fe>H>Cu的结论,不必做补充实验,只需将小明同学方案中插入金属的顺序调整即可,你认为调整后插入金属的顺序是Cu、Fe、Al.
(5)【归纳】比较金属活动性强弱的方法有①利用金属和酸的反应判断金属活动性②利用金属和盐溶液的反应判断金属活动性.
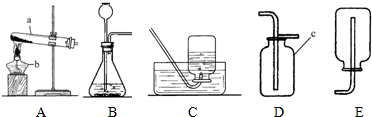
13.如图为初中化学常见气体的发生、收集装置.有关这些装置的说法不正确的是( )
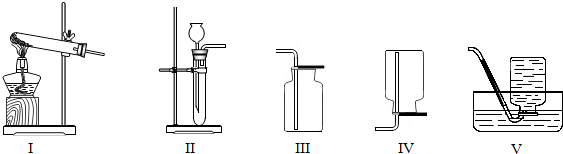

| A. | 装置Ⅰ可作为加热固体制取气体的发生装置 | |
| B. | 装置Ⅱ可用于制取二氧化碳气体,也可以用于制取氧气 | |
| C. | 装置Ⅲ、Ⅳ可用于收集密度与空气密度差距较大,且不与空气中各成分反应色无毒气体 | |
| D. | 装置Ⅳ、Ⅴ都可用于实验室收集氧气 |