题目内容
15.利用铝合金代替铝制钥匙,主要利用铝合金的( )| A. | 密度小 | B. | 熔点低 | C. | 耐腐蚀 | D. | 硬度大 |
分析 合金是指在一种金属中加热熔合其它金属或非金属而形成的具有金属特性的物质;合金的性质是:合金的硬度大,熔点低,耐腐蚀.
解答 解:合金的性质是:合金的硬度大,熔点低,耐腐蚀;合金比组成它的纯金属硬度大,由于纯铝硬度较小,在使用中易变形,因此利用铝合金硬度较大的性质.
故选:D.
点评 本题主要考查合金与合金的性质,合金概念的三个特点要记牢;还要理解合金的性质,即合金的硬度大,熔点低,耐腐蚀.题目难度不大.

练习册系列答案
相关题目
3.某同学开始时视线与量筒内凹液面的最低处相平读数为20mL,倒出一部分液体后,俯视读取剩余液体为12mL,那么他所倒出液体体积为( )
| A. | 大于8mL | B. | 小于8mL | C. | 等于8mL | D. | 无法确定 |
7.下列实验现象描述或作法中正确的是( )
| A. | 细铁丝在纯O2中燃烧,火星四射,生成白色固体,放热 | |
| B. | 稀释浓H2SO4时,将水慢慢注入浓H2SO4里,不断搅拌 | |
| C. | 减少使用一次性木筷,塑料袋,使用无磷洗涤用品,过量使用化肥农药 | |
| D. | 点燃纯净H2时产生淡蓝色火焰,放热 |
4.下列盐不能用金属与稀酸直接反应制得是( )
| A. | MgCl2 | B. | FeCl3 | C. | FeSO4 | D. | AlCl3 |
12.某化学兴趣小组在做完用石灰石和稀盐酸制取二氧化碳的实验后,对反应后的剩余溶液的溶质成分产生了兴趣,他们进行了以下实验探究.
【提出猜想】猜想一:只有CaCl2; 猜想二:CaCl2和HCl.
【实验探究】为了验证猜想,该兴趣小组的同学设计了如下实验方案.
【评价反思】(1)方案1发生反应的化学方程式Fe2O3+6HCl═2FeCl3+3H2O.
(2)有同学提出方案2是错误的,原因是氯化钙和稀盐酸都能够和硝酸银反应生成白色沉淀氯化银.
(3)该兴趣小组的小华同学观察到石灰石和稀盐酸反应后容器内有少量固体剩余,得出溶液中肯定没有盐酸的结论,其他同学认为小华的说法不合理,其理由是剩余的少量固体可能是不能和稀盐酸反应的杂质.
【拓展延伸】石灰石的主要成分碳酸钙可用作补钙剂.某补钙药剂说明书的部分信息如图1所示.现将100g盐酸分成5等份,逐次加到用40片该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与图象如图2.请根据有关信息回答问题.
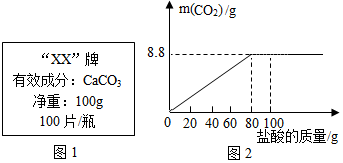
(1)该品牌补钙药剂中CaCO3的质量分数是50%,a的数值为25.
(2)求该盐酸中溶质的质量分数为多少?(写出计算过程,计算结果保留一位小数).
【提出猜想】猜想一:只有CaCl2; 猜想二:CaCl2和HCl.
【实验探究】为了验证猜想,该兴趣小组的同学设计了如下实验方案.
| 方案编号 | 方案1 | 方案2 |
| 实验操作 (分别取少量实验后的溶液于试管中) | 加入少许氧化铁 | 滴加硝酸银溶液 |
| 实验现象 | 固体逐渐消失,溶液由无色变成黄色 | 产生白色沉淀. |
| 实验结论 | 猜想二成立. | |
(2)有同学提出方案2是错误的,原因是氯化钙和稀盐酸都能够和硝酸银反应生成白色沉淀氯化银.
(3)该兴趣小组的小华同学观察到石灰石和稀盐酸反应后容器内有少量固体剩余,得出溶液中肯定没有盐酸的结论,其他同学认为小华的说法不合理,其理由是剩余的少量固体可能是不能和稀盐酸反应的杂质.
【拓展延伸】石灰石的主要成分碳酸钙可用作补钙剂.某补钙药剂说明书的部分信息如图1所示.现将100g盐酸分成5等份,逐次加到用40片该药剂制成的粉末中(其他成分不与盐酸反应),得到部分数据与图象如图2.请根据有关信息回答问题.

| 第1次 | 第3次 | 第4次 | |
| 加入盐酸的质量(g) | 20 | 20 | 20 |
| 剩余固体的质量(g) | 35 | a | 20 |
(2)求该盐酸中溶质的质量分数为多少?(写出计算过程,计算结果保留一位小数).