题目内容
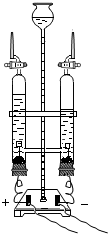
12.某化学兴趣小组设计了一组“吹气球”实验,三套装置如图:
(1)甲装置:仪器a的名称为长颈漏斗;向a中加水至浸没长颈漏斗管口,可以观察到的现象是气球变大.
(2)乙装置:若生成H2使气球胀大,实验室一般用稀硫酸与金属Zn制取氢气,而不用稀盐酸的原因是稀盐酸易挥发出氯化氢气体,其反应的化学方程式为Zn+H2SO4═ZnSO4+H2↑;若锥形瓶中装有CaO固体,分液漏斗中加入少量水,则气球胀大的主要原因是氧化钙与水反应生成了氢氧化钙,放出了大量的热.
(3)丙装置:若锥形瓶中盛满CO2,欲使气球胀大,则分液漏斗中的液体可以是氢氧化钠溶液.
分析 观察实验的装置图,根据压强的变化分析气球的变化,盐酸易挥发出氯化氢气体,氧化钙能与水反应生成了氢氧化钙放出了大量的热,氢氧化钠能与二氧化碳反应.
解答 解:(1)甲装置:仪器a的名称为长颈漏斗;向a中加水至浸没长颈漏斗管口,瓶内气体体积减小,压强增大,可以观察到的现象是气球变大.
(2)乙装置:若生成H2使气球胀大,实验室一般用稀硫酸与金属Zn制取氢气,而不用稀盐酸的原因是稀盐酸易挥发出氯化氢气体,其反应的化学方程式为:Zn+H2SO4═ZnSO4+H2↑;若锥形瓶中装有CaO固体,分液漏斗中加入少量水,则气球胀大的主要原因是:氧化钙与水反应生成了氢氧化钙,放出了大量的热.
(3)丙装置:若锥形瓶中盛满CO2,欲使气球胀大,则分液漏斗中的液体可以是氢氧化钠溶液,氢氧化钠能吸收二氧化碳,瓶内压强减小,大气压使小球变大.
故答为:(1)长颈漏斗,气球变大;(2)稀盐酸易挥发出氯化氢气体,Zn+H2SO4═ZnSO4+H2↑;氧化钙与水反应生成了氢氧化钙,放出了大量的热.(3)氢氧化钠溶液.
点评 此题的难度不大,掌握实验室制取氧气的原理以及二氧化碳的性质等即可顺利解答此题.

练习册系列答案
 寒假大串联黄山书社系列答案
寒假大串联黄山书社系列答案
相关题目
7.用“ ”和“
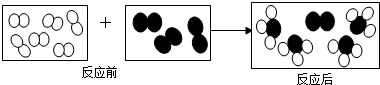
”和“ ”代表两种不同的单质分子,它们在一定条件下能发生化学反应,反应前后的微观示意图如图所示,下列说法正确的是( )
”代表两种不同的单质分子,它们在一定条件下能发生化学反应,反应前后的微观示意图如图所示,下列说法正确的是( )
 ”和“
”和“ ”代表两种不同的单质分子,它们在一定条件下能发生化学反应,反应前后的微观示意图如图所示,下列说法正确的是( )
”代表两种不同的单质分子,它们在一定条件下能发生化学反应,反应前后的微观示意图如图所示,下列说法正确的是( )
| A. | 该反应可能不是化合反应 | |
| B. | 每个生成物分子由3个原子构成 | |
| C. | 该反应有2种生成物 | |
| D. | 参加反应的两种反应物分子个数比为3:1 |
17.如图所示为W原子和Y原子的原子结构示意图.下列说法错误的是( )


| A. | Y的原子结构示意图中x为12 | |
| B. | W原子和Y原子分别属于非金属原子和金属原子 | |
| C. | W原子和Y原子分别形成简单离子的过程相同 | |
| D. | W原子与Y原子分别形成的离子可构成新的物质--YW2 |
4.下列变化,属于化学变化的是( )
| A. | 澄清石灰水久置变浑浊 | B. | 酒精挥发 | ||
| C. | 锅炉爆炸 | D. | 矿石粉碎 |
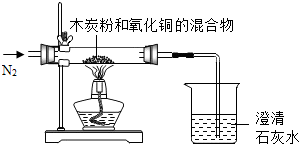 某同学设计一个实验,证明氧化铜中含有氧元素,并测定氧化铜中氧元素的质量分数,实验装置如下图.
某同学设计一个实验,证明氧化铜中含有氧元素,并测定氧化铜中氧元素的质量分数,实验装置如下图.
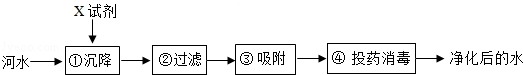
 水是人及一切生物所必需的,为了人类和社会经济的可持续发展,我们应该了解有关水的一些知识.请你回答:
水是人及一切生物所必需的,为了人类和社会经济的可持续发展,我们应该了解有关水的一些知识.请你回答: