题目内容
向某铁粉样品中,加入溶质质量分数为20%的硫酸铜溶液80g,恰好完全反应(样品中杂质不溶于水也不与硫酸铜反应),请结合图提供的数据计算:
(1)b的数值;
(2)向不饱和滤液中加入120.8g水,求所得溶液中溶质的质量分数.

| 根据化学反应方程式的计算;有关溶质质量分数的简单计算. | |
| 专题: | 综合计算(图像型、表格型、情景型计算题). |
| 分析: | (1)根据硫酸铜的质量求出参加反应铁的质量和生成铜的质量,从而求出a的数值进行解答; (2)根据溶质质量分数公式进行解答. |
| 解答: | 解: (1)设:样品中铁的质量为x,生成铜的质量为y,生成硫酸亚铁的质量为z. 硫酸铜的质量=80g×20%=16g Fe+CuSO4=FeSO4+Cu 56 160 152 64 x 16g z y
x=5.6g
z=15.2g
b=5.6g+(7g﹣6.4g)=6.2g (2)加入水后溶液的质量=80g+5.6g﹣6.4g+120.8g=200g 所得溶液中溶质的质量分数 答案: (1)b的数值为6.2g. (2)向不饱和滤液中加入120.8g水,所得溶液中溶质的质量分数为7.6%. |
| 点评: | 掌握化学方程式的计算格式和规范性,本题的难点是(1)的计算,一定要考虑杂质的质量. |

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案下列实验方案中,不能达到实验目的是( )
| 选项 | 实验目的 | 实验方案 |
| A | 鉴别硬水和软水 | 加肥皂水搅拌 |
| B | 除去氯化钠固体中的少量碳酸钠 | 加入适量稀盐酸,充分反应后,蒸发 |
| C | 分离碳酸钠和氢氧化钠的混合物 | 加入过量氯化钙溶液,过滤 |
| D | 区分羊毛与合成纤维 | 点燃,闻气味 |
|
| A. | A | B. | B | C. | C | D. | D |
下列各组物质的鉴别方法不能够达到预期目的的是
| 编号 | 被鉴别物质 | 鉴别方法 |
| A | O2与CO2 | 分别通入澄清石灰水中 |
| B | HCl与H2SO4 | 分别滴加BaCl2溶液 |
| C | Ca(OH)2溶液与Na2CO3溶液 | 分别滴加酚酞试液 |
| D | CuCl2溶液与Cu(NO3)2溶液 | 分别滴加AgNO3溶液 |
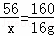
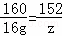
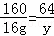
 y=6.4g
y=6.4g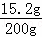 ×100%=7.6%
×100%=7.6%