题目内容
15.现有仪器:量筒、玻璃棒、药匙、托盘天平、蒸发皿、胶头滴管.请回答:(1)用于称量固体药品的是托盘天平;
(2)取用固体药品的是药匙;
(3)量取液体体积的是量筒;
(4)可用于搅拌液体的是玻璃棒;
(5)用于吸取和滴加少量液体的是胶头滴管.
分析 在了解各个仪器作用的基础上,对号入座即可.
(1)托盘天平用于固体药品的称量;
(2)药匙用于固体药品的取用;
(3)量筒用于量取一定液体的体积;
(4)玻璃棒可用于液体的搅拌;
(5)胶头滴管能够用于吸取和滴加少量液体.
解答 解:(1)托盘天 平用于固体药品的称量,用托盘天平称量物品,要遵循“左物右码”的原则;
(2)药匙:用于取用粉末或小粒状的固体药品,每次用前要将药匙用干净的滤纸揩净;
(3)量筒:用于量取一定量体积液体的仪器;
(4)玻璃棒:用做搅拌(加速溶解)液体,过滤或配置溶液时帮助转移液体,在倾泻时引流液体,蘸取液体使之与试纸作用;
(5)胶头滴管:用于吸取和滴加少量液体.
故答案为:(1)托盘天平.
(2)药匙.
(3)量筒.
(4)玻璃棒.
(5)胶头滴管.
点评 本题主要考查常见实验仪器的作用,是较为简单的题型,只要同学们在平时的学习中稍加留心即可做好.

练习册系列答案
 优生乐园系列答案
优生乐园系列答案 新编小学单元自测题系列答案
新编小学单元自测题系列答案
相关题目
6.下表中 代表氢原子,
代表氢原子, 代表氧原子,
代表氧原子, 代表碳原子,则下列有关说法不正确的是( )
代表碳原子,则下列有关说法不正确的是( )
 代表氢原子,
代表氢原子, 代表氧原子,
代表氧原子, 代表碳原子,则下列有关说法不正确的是( )
代表碳原子,则下列有关说法不正确的是( )| 物质 | ① | ② | ③ | ④ |
| 分子模型 示意图 |  |  |  |  |
| A. | 上述物质中,①是单质 | |
| B. | 物质②的相对分子质量为18 | |
| C. | 上述物质中,③中氧元素质量分数最大 | |
| D. | 物质③和④组成的元素相同 |
3.四名同学的对话,你同意谁的说法( )
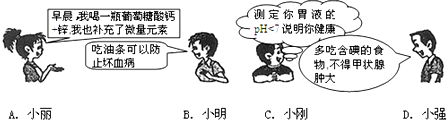

| A. | A | B. | B | C. | C | D. | D |
10.我国制碱工业的先驱侯德榜将制碱与制氨结合起来的联合制碱法,为纯碱和氮肥工业技术的发展做出了杰出的贡献.其生产工艺流程示意图如下:
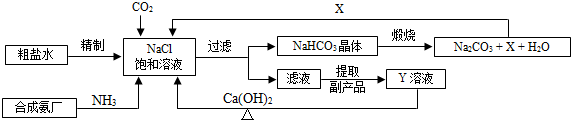
(1)粗盐水中主要含有Ca2+、Mg2+、SO42-等杂质离子,工业上常用加入稍过量的NaOH溶液、Na2CO3溶液、BaCl2溶液及适量的盐酸等除杂、精制.则加入试剂合理的顺序为NaOH溶液、BaCl2溶液、Na2CO3溶液或BaCl2溶液、NaOH溶液、Na2CO3溶液、盐酸(只写一种).加盐酸的作用是(用化学方程式表示)Na2CO3+2HCl═2NaCl+H2O+CO2↑、HCl+NaOH═NaCl+H2O.
(2)制碱原理为:NaCl+CO2+NH3+H2O=NaHCO3↓+NH4Cl,该反应原理可看作是由①CO2+NH3+H2O═NH4HCO3和②NaCl+NH4HCO3═NaHCO3↓+NH4Cl两个反应加合而成,则反应类型为复分解反应.
(3)X的化学式为CO2.
(4)Y是滤液中的最主要成分,Y与Ca(OH)2反应的产物之一可用于循环使用,该产物的名称为氯化铵,Y的化学式为NH4Cl,写出Y的一种用途氨气.

(1)粗盐水中主要含有Ca2+、Mg2+、SO42-等杂质离子,工业上常用加入稍过量的NaOH溶液、Na2CO3溶液、BaCl2溶液及适量的盐酸等除杂、精制.则加入试剂合理的顺序为NaOH溶液、BaCl2溶液、Na2CO3溶液或BaCl2溶液、NaOH溶液、Na2CO3溶液、盐酸(只写一种).加盐酸的作用是(用化学方程式表示)Na2CO3+2HCl═2NaCl+H2O+CO2↑、HCl+NaOH═NaCl+H2O.
| OH- | SO42- | CO32- | |
| Mg2+ | 不 | 溶 | 微 |
| Ca2+ | 微 | 微 | 不 |
| Ba2+ | 溶 | 不 | 不 |
(3)X的化学式为CO2.
(4)Y是滤液中的最主要成分,Y与Ca(OH)2反应的产物之一可用于循环使用,该产物的名称为氯化铵,Y的化学式为NH4Cl,写出Y的一种用途氨气.
7.下列做法不利于减少空气污染的是( )
| A. | 在我国西北地区加快植树造林,减少半荒漠化土地 | |
| B. | 城市中实施集中供暖,取缔小锅炉 | |
| C. | 实施新的更严格的汽车排放标准 | |
| D. | 过年时家家户户大放烟花爆竹 |
4. 红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究.
红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究.
【提出问题】久置固体的成分是什么?
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁.
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2、CaCO3.
久置固体中可能含有Ca(OH)2的原因是:用化学方程式表示CaO+H2O=Ca(OH)2.
【实验探究】甲同学的方案(见表).
【实验质疑】
(1)乙同学认为甲同学的实验中的实验中不能得出一定含有Ca(OH)2的结论,理由是氧化钙与水反应会生成氢氧化钙,也能使无色酚酞变红,不能确定原固体中是否有氢氧化钙;
(2)丙同学认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是氧化铁与盐酸反应生成氯化铁,铁与氯化铁溶液在常温下发生反应也会生成氯化亚铁,使溶液显浅绿色.
 红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究.
红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图所示.同学们对一包久置的“504双吸剂”固体样品很好奇,设计实验进行探究.【提出问题】久置固体的成分是什么?
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁.
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2、CaCO3.
久置固体中可能含有Ca(OH)2的原因是:用化学方程式表示CaO+H2O=Ca(OH)2.
【实验探究】甲同学的方案(见表).
| 实验操作 | 实验现象 | 实验结论 |
| (1)取少量固体放于试管中,加足量蒸馏水溶解,静置后取上层清液滴加无色酚酞溶液 | 固体溶解时试管外壁发烫,试管底部有不溶物,溶液变红 | 固体中一定含有氧化钙 和氢氧化钙 |
| (2)另取少量固体放于试管中,滴加足量的稀盐酸 | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液 | 固体中一定含有铁,一定不含有Fe2O3 |
| (3)将步骤(2)中产生的气体通入到澄清石灰水中 | 澄清的石灰水变浑浊 | 固体中一定含有CaCO3 |
(1)乙同学认为甲同学的实验中的实验中不能得出一定含有Ca(OH)2的结论,理由是氧化钙与水反应会生成氢氧化钙,也能使无色酚酞变红,不能确定原固体中是否有氢氧化钙;
(2)丙同学认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是氧化铁与盐酸反应生成氯化铁,铁与氯化铁溶液在常温下发生反应也会生成氯化亚铁,使溶液显浅绿色.
5.下列变化中,属于分解反应的是( )
| A. | 铜+氧气$\stackrel{加热}{→}$氧化铜 | B. | 石蜡+氧气$\stackrel{点燃}{→}$水+二氧化碳 | ||
| C. | 过氧化氢$\stackrel{MnO_2}{→}$水+氧气 | D. | 铁+氧气$\stackrel{点燃}{→}$四氧化三铁 |