题目内容
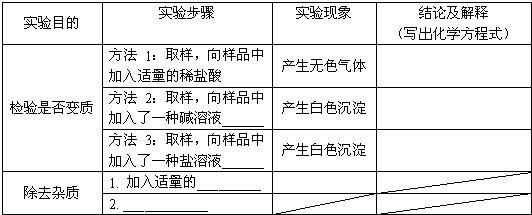
某实验室把氢氧化钠浓溶液暴露在空气中一段时间,实验员猜测氢氧化钠浓溶液已部分变质.于是他进行了以下实验:| 实验目的 | 实验步骤 | 实验现象 | 结论及解释 (写出化学方程式) |
| 检验是否变质 | 方法1:取样,向样品只加入适量的稀盐酸 | 产生无色气体 | |
| 方法2:取样,向样品中加入了一种碱溶液_____________ | 产生白色沉淀 | ||
| 方法3:取样,向样品中加入一种盐溶液 ______________ | 产生白色沉淀 | ||
| 除去杂质 | 1.加入适量的____ | 白色沉淀 | 此空不填写 |
| 2.______________ | 此空不填写 | 此空不填写 |
【答案】分析:氢氧化钠若变质,则会生成碳酸钠,所以这里我们检验氢氧化钠是否变质,主要验证是不是存在着碳酸钠,检验碳酸盐常用的物质有盐酸、含有钙离子或钡离子的碱或盐,可以据此解答该题.
解答:解:方法1:加入盐酸生成了气体,则该气体是二氧化碳,所以发生的反应为盐酸和碳酸钠的反应
方法2:根据实验现象可以知道加入的碱能够和碳酸钠反应生成沉淀,能够和碳酸钠反应生成沉淀的碱为氢氧化钙或是氢氧化钡.故可以写出反应的化学方程式
方法3:向样品中加入盐后生成了沉淀,可知加入的应该是氯化钙或是氯化钡,故可以写出该反应的化学方程式
除去杂质常用氢氧化钙溶液使碳酸根离子转化为沉淀,然后过滤即可.
结论:根据实验现象可以看出该氢氧化钠溶液已经变质
故答案为:
(2)结论:已部分变质生成Na2CO3
点评:熟练掌握氢氧化钠的性质以及碳酸根的检验方法,注意检验碳酸根离子时,所用的试剂在发生化学反应时必须有明显的实验现象.
解答:解:方法1:加入盐酸生成了气体,则该气体是二氧化碳,所以发生的反应为盐酸和碳酸钠的反应
方法2:根据实验现象可以知道加入的碱能够和碳酸钠反应生成沉淀,能够和碳酸钠反应生成沉淀的碱为氢氧化钙或是氢氧化钡.故可以写出反应的化学方程式
方法3:向样品中加入盐后生成了沉淀,可知加入的应该是氯化钙或是氯化钡,故可以写出该反应的化学方程式
除去杂质常用氢氧化钙溶液使碳酸根离子转化为沉淀,然后过滤即可.
结论:根据实验现象可以看出该氢氧化钠溶液已经变质
故答案为:
| 实验目的 | 实验步骤 | 实验现象 | 结论及解释 (写出化学方程式) |
| 检验是否变质 | 方法1:取样,向样品只加入适量的稀盐酸 | 产生无色气体 | Na2CO3+2HCl=2NaCl+H2O +CO2↑ |
| 方法2:取样,向样品中加入了一种碱溶液_ Ca(OH)2 | 产生白色沉淀 | Na2CO3+Ca(OH)2=CaCO3↓+2NaOH | |
| 方法3:取样,向样品中加入一种盐溶液 CaCl2或BaCl2 | 产生白色沉淀 | CaCl2+Na2CO3=CaCO3↓+2NaCl 或 BaCl2+Na2CO3=BaCO3↓+2NaCl | |
| 除去杂质 | 1.加入适量的Ca(OH)2 | 白色沉淀 | |
| 2.过滤 |
点评:熟练掌握氢氧化钠的性质以及碳酸根的检验方法,注意检验碳酸根离子时,所用的试剂在发生化学反应时必须有明显的实验现象.

练习册系列答案
 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案
相关题目
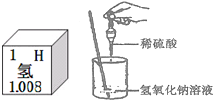 酸、碱、盐是初中化学学习的重要内容,同学们在实验室对酸、碱、盐的性质进行探究.
酸、碱、盐是初中化学学习的重要内容,同学们在实验室对酸、碱、盐的性质进行探究.