题目内容
5.根据初中所学的知识并结合如图1仪器回答问题: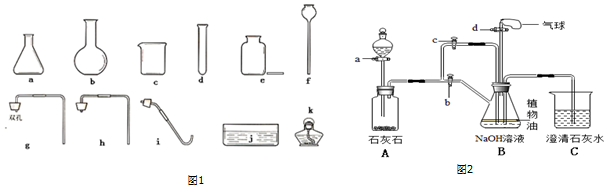
(1)实验室选取d、e、i、j、k五种仪器用高锰酸钾制取氧气,其中还缺少的仪器是铁架台,反应的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,实验中发现j中水变红,原因是试管口没有棉花团.
(2)若用a、h、e制取氧气的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,检验氧气收集满的方法是先把导管的一端放入水中,然后两手紧握试管的外壁,观察导管口是否有气泡冒出.
(3)小明同学在实验室用浓盐酸与大理石制取二氧化碳,组装发生装置除选用了仪器b、g 外,还需选择上述仪器中的长颈漏斗(写名称),其作用是方便加液体药品.反应的化学方程式是CaCO3+2HCl=CaCl2+H2O+CO2↑.向集气瓶中倒入澄清石灰水,发现澄清石灰水溶液不变浑浊,造成这一现象的可能原因是二氧化碳中混有浓盐酸挥发出来的氯化氢气体.
(4)小王和小李两位同学用如图2所示装置进行制取二氧化碳并验证其与氢氧化钠能发生反应.
①小王先关闭b,打开a、c、d,使分液漏斗中的液体缓慢滴入,A中缓慢出现气泡,B中没有观察到明显现象.
②小李认为若要证明NaOH与CO2发生了化学反应,接下来的操作是关闭c、d,打开a、b,B中液体压入C中,
此时观察到C装置中的石灰水变浑浊,写出该反应的化学方程式Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
分析 检验装置的气密性的方法是:先把导管的一端放入水中,然后两手紧握试管的外壁,观察导管口是否有气泡冒出.制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.小李认为若要证明NaOH与CO2发生了化学反应,接下来的操作是:关闭c、d,打开a、b,B中液体压入C中,此时观察到C装置中的石灰水变浑浊,因为碳酸钠和氢氧化钙反应生成碳酸钙白色沉淀和氢氧化钠,配平即可.
解答 解:(1)实验室选取d、e、i、j、k五种仪器用高锰酸钾制取氧气,其中还缺少的仪器是铁架台;高锰酸钾受热分解生成锰酸钾和二氧化锰和氧气,要注意配平;加热高锰酸钾时,试管口要放一团棉花,是为了防止高锰酸钾粉末进入导管;故答案为:铁架台;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;试管口没有棉花团;
(2)如果用双氧水和二氧化锰制氧气就不需要加热,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,要注意配平;检验装置的气密性的方法是:先把导管的一端放入水中,然后两手紧握试管的外壁,观察导管口是否有气泡冒出;故答案为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;先把导管的一端放入水中,然后两手紧握试管的外壁,观察导管口是否有气泡冒出;
(3)长颈漏斗方便加液体药品,碳酸钙和盐酸反应生成氯化钙和水和二氧化碳,配平即可;向集气瓶中倒入澄清石灰水,发现澄清石灰水溶液不变浑浊,造成这一现象的可能原因是:二氧化碳中混有浓盐酸挥发出来的氯化氢气体;故答案为:长颈漏斗;方便加液体药品;CaCO3+2HCl=CaCl2+H2O+CO2↑;二氧化碳中混有浓盐酸挥发出来的氯化氢气体;
(4)小李认为若要证明NaOH与CO2发生了化学反应,接下来的操作是:关闭c、d,打开a、b,B中液体压入C中,此时观察到C装置中的石灰水变浑浊,因为碳酸钠和氢氧化钙反应生成碳酸钙白色沉淀和氢氧化钠,配平即可;故答案为:关闭c、d,打开a、b,B中液体压入C中;Na2CO3+Ca(OH)2=CaCO3↓+2NaOH;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和气体的性质等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

| A. |  倾倒液体 | B. |  加热液体 | C. |  量取液体 | D. |  滴加液体 |
| A. | 剩余固体为混合物 | |
| B. | 剩余固体中钠元素的为4.6g | |
| C. | 反应生成CO2的质量为3.1g | |
| D. | 加热前后的固体分别与相同浓度稀盐酸恰好完全反应所消耗盐酸质量相等 |
| A. | 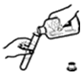 倾倒液体 | B. | 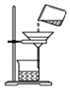 过滤 | C. | 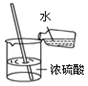 稀释浓硫酸 | D. | 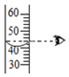 量取水的体积 |
| A. |  活性炭净水 | B. |  金刚石作装饰品 | C. |  铜丝作导线 | D. |  氢气作高能燃料 |
| A. | 合金:生铁、锰钢、青铜 | |
| B. | 碱:纯碱、烧碱、消石灰 | |
| C. | 盐:氯化铵、氯化钠、氯化氢 | |
| D. | 合成材料:塑料、合成纤维、天然橡胶 |
| A | 氧化物 | NO | H2O2 | KClO3 |
| B | 污染物 | CO | PM2.5 | SO2 |
| C | 有机物 | 乙炔 | 石油 | 乙醇 |
| D | 纯净物 | 纯碱 | 硫酸 | 熟石灰 |
| A. | A | B. | B | C. | C | D. | D |
| A. | 大量植树造林,禁止乱砍滥伐 | |
| B. | 夏天为了更凉快,把室内空调温度设置到很低 | |
| C. | 家庭电器长期处于待机状态 | |
| D. | 尽量乘坐公交车或骑自行车出行 |
| A. |  | B. |  | C. |  | D. |  |