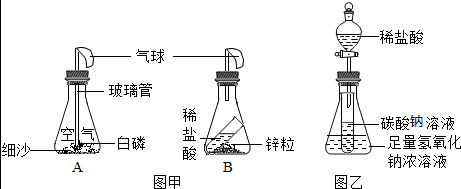
��Ŀ����
13������������ǧ�����������������Ҫ��Դ���⣬ͼ1�Ǻ�ˮ�л�ѧ��Դ��ͼʾ������ͼʾ�ش�������⣮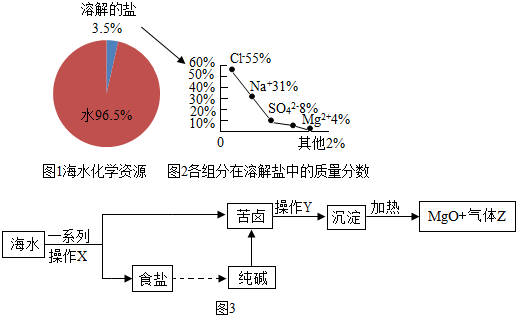
��1��ȡ��ˮ�μ�AgNO3��Һ���������а�ɫ�������ɣ�
��2�������йغ�ˮ���俪����˵����ȷ����ad��
a��ͼ2�к�ˮ������ѧ��Դ���ǻ�����
b����������ˮ�ǻ�ѧ�仯
c����ˮ��Դ�Ŀ�������Ҫ���ǻ�����������
d����ˮ�к���NaCl��MgCl2
��3����ˮ�к���10�����ӵ�����H2O��Mg2+��Na+��
��4����ҵ���ú�ˮ��ȡ���������MgO������ͼ��ͼ3����ͼ�ش��������⣮
��MgO������������þ��
�ں�ˮɹ�ε�һϵ�в���X���������ᾧ�����ˣ�ʵ���ҽ��в���Yʱ��ʹ�ò����������������������۰����ȡ���������Ƴɱ��Ͱ���ˮ���ٲ���ͨ�������̼����Ӧ����̼�����ƺ��Ȼ�泥���������̼�����Ƶ�ԭ������ͬ�����£�̼�����Ƶ��ܽ��С���Ȼ�淋��ܽ�ȣ�̼�����Ʒֽ����ɴ���Ļ�ѧ����ʽ��2NaHCO3$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+H2O+CO2����
�ܿ�±����MgCl2��NaCl�����봿��ķ�Ӧ�����Ǹ��ֽⷴӦ��
��2.4��105t��ˮ�к�þԪ�ص�������336t��������ʵ�ʵõ�523.6t����Z�������������MgO�IJ��ʣ�д����Ҫ�ļ�����̣�
����֪������=$\frac{ʵ�ʵõ��IJ�������}{�����ϵIJ�������}$��100%���������ϵIJ����������Dz�������ʧ���ҷ�Ӧ����ȫ��Ӧʱ�IJ���������
���� ��1���������������������ӽ�ϳ��Ȼ���������������
��2�����ݺ�ˮ�����������Լ���ˮ������ע��������������
��3��������������������������
��4���ٸ��������������������������
�ڸ��ݺ�ˮɹ�ε�ԭ���Լ���������������������
����ͬ�����£����ʵ��ܽ��ԽС��Խ���״���Һ����������ϻ�ѧ����ʽ��д����������
�ܸ��ݷ�Ӧ���͵��жϷ�����������
�ݸ���þԪ�صĺ����Լ���ѧ����ʽ�ļ������������
��� �⣺��1����ˮ�к��������ӣ���ˮ�еμ���������Һ���������������ӽ�ϳ��Ȼ�����ɫ����������а�ɫ�������ɣ�
��2��a����ͼ2��֪����ˮ�к��е����ʶ��ǻ�������Ȼ�þ���Ȼ��ơ�����þ�������Ƶȣ�����ȷ��
b����ˮ�к���ˮ����˺�ˮ�ĵ���û�����������ʣ����������������仯���ʴ���
c����ˮ��Դ�Ŀ����Ĺ�����Ҫ���ǻ������⣬���ܶԻ��������Ⱦ���ʴ���
d����ͼ2��Ϣ��֪����ˮ�к����Ȼ�þ���Ȼ��ơ�����þ�������Ƶ����ʣ�����ȷ��
��ѡad��
��3����ԭ�Ӻ�����11�����ӣ�ʧȥ������1�����Ӷ��γ������ӣ�������10�����ӣ����Na+��
��4�����������������������֪��MgO��������þ���������þ��
�ں�ˮɹ�εĹ������������ᾧ�����ˣ�����Y�Ƿ���������ʵIJ������ǹ��ˣ��ڹ��˲����в�����������������������ᾧ��������
�۰���ˮ���ն�����̼�����ɵ�̼�����ƺ��Ȼ�泥����Ƚᾧ������������̼�ᰱ�ƣ���ԭ������ͬ�����£�̼�����Ƶ��ܽ��С���Ȼ�淋��ܽ�ȣ������ͬ�����£�̼�����Ƶ��ܽ��С���Ȼ�淋��ܽ�ȣ�̼���������ȷֽ�����̼���ơ�ˮ�Ͷ�����̼����Ӧ�Ļ�ѧ����ʽΪ��2NaHCO3$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+H2O+CO2����
�ʴ�Ϊ����ͬ�����£�̼�����Ƶ��ܽ��С���Ȼ�淋��ܽ�ȣ�2NaHCO3$\frac{\underline{\;\;��\;\;}}{\;}$Na2CO3+H2O+CO2����
�ܿ�±����MgCl2��NaCl�����봿����Ȼ�����̼���Ʋ���Ӧ�������Ȼ�þ��̼���Ʒ�Ӧ�����Ȼ��ƺ�̼��þ�������������ֻ�����������ɷַ����������µĻ�������ڸ��ֽⷴӦ��������ֽⷴӦ��
��2.4��105t��ˮ�к�þԪ�ص�������2.4��105t��3.5%��4%=336t������������������þ������Ϊ��336t��$\frac{24}{40}��100%$=560t�����336��
̼��þ���ȷֽ�Ϊ����þ�Ͷ�����̼������������þ������Ϊx
MgCO3$\frac{\underline{\;\;��\;\;}}{\;}$MgO+CO2��
40 44
x 523.6t
$\frac{40}{44}=\frac{x}{523.6t}$
x=476t
������MgO�IJ�����$\frac{476t}{560t}��100%$=85%
��������MgO�IJ���Ϊ85%��
���� �����Ժ�����Դ������Ϊ���壬����Ժ�ˮ�ĺ������������ã���ѧ��Դ������������ַ�����������������ҵ�dz��л�ѧ��Ҫ��Ӧ��֮һ���ǿ����ص㣬���漰��ѧ����ʽ����д����Ӧʱ����̼�����Ƶ�ԭ���������ܽ�ȵĹ�ϵ��

����Һ��ֻ����FeSO4 ����Һ�к���FeSO4��ZnSO4 ��������һ������Zn��Fe��Cu ��������ֻ����Fe��Cu������������һ������ԭ���۵����� ������������һ��С��ԭ���۵�������
| A�� | ֻ�Т٢� | B�� | ֻ�Тڢ� | C�� | ֻ�Тڢ� | D�� | ֻ�Тۢ� |
| A�� |  ���װ�������� | B�� |  �μ�Һ�� | C�� |  �ܽ���� | D�� |  Ϩ��ƾ��� |
| ��ѧ����ʽ | ��Ӧ���� | |
| A | CO+O2�TCO2 | ���Ϸ�Ӧ |
| B | 2KMnO4$\frac{\underline{\;\;��\;\;}}{\;}$K2MnO2+MnO2+2O2�� | �ֽⷴӦ |
| C | 2Ag+H2SO4�TAg2SO4+H2�� | �û���Ӧ |
| D | CuSO4+BaCl2�TCuCl2+BaSO4�� | ���ֽⷴӦ |
| A�� | A | B�� | B | C�� | C | D�� | D |
����ʢ��5mL 5%����������Һ���Թ��У���������ǵ�ľ����ľ������ȼ
����ʢ��5mL w%����������Һ���Թ��У�����ag�������̣���������ǵ�ľ����ľ����ȼ
����ʢ��5mL w%����������Һ���Թ��У�����ag��������������������ǵ�ľ����ľ����ȼ
�ܾ����飬�ڡ����з�Ӧ���Թ��зֱ���ag�������̺�ag������������
���⣺��1���������̺�������������������Ӧ�е����ÿ����Ǵ�����
��2������ʵ����ֻ�м���֤���˶������̺������������������ͻ�ѧ���ʲ��䣬���� ����֤�������ڷ�Ӧ�е����ã�
��3��ʵ��ڡ����й��������Ũ�ȣ�w%����5%Ϊ�ˣ�
�о�С�黹����ҺŨ�ȡ������������ʵ������������̽�����±�ѡȡ�˲���ʵ�����ݣ�
���������������������Һ��ȡ��ͬ������������ʱ��
| 30%�������� | 15%�������� | 5%�������� | |
| ����a g�������� | 0.2�� | 0.8�� | 2.0�� |
| ����a g���������� | 7.0�� | 9.0�� | 16.0�� |
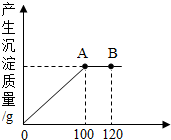
 ��ͼ��a��b��c�������ʵ��ܽ�����ߣ���ش��������⣮
��ͼ��a��b��c�������ʵ��ܽ�����ߣ���ش��������⣮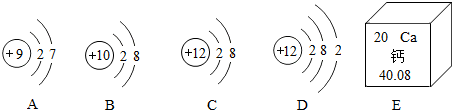
 ����Ա��ѧУʵ���ҷ�����һƿ���ڷ��õ�����������Һ��ͬѧС����Ϊ����Һ�Ѳ��ֱ��ʳ�Na2CO3��Ϊ̽����Һ�����ʵijɷ֣���ش��������⣮
����Ա��ѧУʵ���ҷ�����һƿ���ڷ��õ�����������Һ��ͬѧС����Ϊ����Һ�Ѳ��ֱ��ʳ�Na2CO3��Ϊ̽����Һ�����ʵijɷ֣���ش��������⣮