题目内容
17.如图是有关氧气的知识网络图(部分反应条件已略去).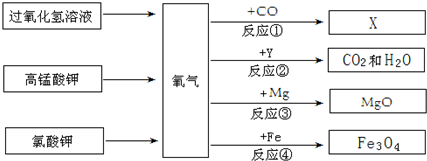
根据上图回答下列问题:
(1)生成氧气的三个反应都属于分解反应(填基本反应类型).
(2)X的化学式为CO2. X可灭火的原理是二氧化碳不燃烧也不能支持燃烧.
(3)Y是一种可再生能源,也可称为绿色能源,Y的化学式为C2H5OH.
(4)在反应③的实验中可以观察到的实验现象是剧烈燃烧、发出耀眼白光,生成白色固体.
(5)在做反应④实验时,要预先在盛放氧气的集气瓶中放少量水的原因是防止反应产生的高温熔落物炸裂瓶底.
分析 (1)根据反应的化学方程式,结合基本反应类型的定义和特点进行解答.
(2)根据碳和氧气的反应,注意反应条件不同,产物也不同.
(3)根据质量守恒定律以及可再生资源分析.
(4)根据磷燃烧现象分析.
(5)根据铁丝在氧气中燃烧的注意事项分析.
解答 解:(1)由于双氧水、高锰酸钾以及氯酸钾分解能产生氧气的反应均是反应物是一种,而生成物是多种,所以这三个反应均是分解反应;
(2)一氧化碳与氧气反应会生成二氧化碳(CO2),由于二氧化碳不燃烧也不能支持燃烧,所以二氧化碳能用来灭火;
(3)Y的燃烧会生成二氧化碳和水,所以Y可能是有机物,由于该物质的可再生资源,所以Y可以是酒精,化学式为C2H5OH;
(4)实验③是镁条的燃烧反应,其反应时能观察到的现象是剧烈燃烧、发出耀眼白光,生成白色固体;
(5)实验④是铁丝的燃烧反应,实验时为防止反应产生的高温熔落物炸裂瓶底,所以要预先在盛放氧气的集气瓶中放少量水;
故答案为:(1)分解;
(2)CO2;二氧化碳不燃烧也不能支持燃烧;
(3)C2H5OH;
(4)剧烈燃烧、发出耀眼白光,生成白色固体;
(5)防止反应产生的高温熔落物炸裂瓶底.
点评 本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力.增加了学生分析问题的思维跨度,强调了学生整合知识的能力.

练习册系列答案
相关题目
8.某化学实验小组用如图所示的装置模拟工业炼铁的原理,请你参与探究:
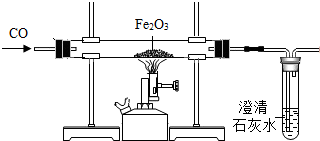
【初步探究】请写出工业上用赤铁矿(主要成分是Fe2O3)炼铁的主要原理的化学方程式:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,如图装置中的一处明显错误是没有处理尾气.实验中,待Fe2O3完全变成黑色粉末时停止加热,继续通入CO至装置冷却到室温,为检验生成物的组成,取适量黑色粉末加入足量的硫酸铜溶液,充分反应,黑色粉末中只有少量的红色固体产生.
【提出问题】黑色粉末可能是什么呢?
【查阅资料】1工业上用赤铁矿炼铁的过程分为三个阶段:
①3Fe2O3+CO$\frac{\underline{\;500-600℃\;}}{\;}$2Fe3O4+CO2;
②Fe3O4+CO$\frac{\underline{\;600-700℃\;}}{\;}$3FeO+CO2;
③FeO+O$\frac{\underline{\;>700℃\;}}{\;}$Fe+CO2
2铁的氧化物和硫酸铜溶液不反应,但都能与盐酸反应,其中除Fe2O3,为红棕色外,其余都为黑色,并且只有Fe3O4,能被磁铁吸引.
【猜想假设】小组同学一致认为黑色粉末一定是含有Fe的混合物,因为只有铁能和硫酸铜反应生成红色固体铜,并提出如下猜想:猜想1:黑色粉末是Fe和FeO,猜想2:黑色粉末是Fe和Fe3O4;猜想3:黑色粉末是Fe、FeO和Fe3O4.
【实验探究】小组同学经过思考、实验、合作和交流,最后得出猜想1成立的结论,下面是甲、乙两同学各自设计的一套验证猜想1的实验方案,请把表格补充完整.
【思维拓展】请设计实验方案,验证猜想2、3的正确性.

【初步探究】请写出工业上用赤铁矿(主要成分是Fe2O3)炼铁的主要原理的化学方程式:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,如图装置中的一处明显错误是没有处理尾气.实验中,待Fe2O3完全变成黑色粉末时停止加热,继续通入CO至装置冷却到室温,为检验生成物的组成,取适量黑色粉末加入足量的硫酸铜溶液,充分反应,黑色粉末中只有少量的红色固体产生.
【提出问题】黑色粉末可能是什么呢?
【查阅资料】1工业上用赤铁矿炼铁的过程分为三个阶段:
①3Fe2O3+CO$\frac{\underline{\;500-600℃\;}}{\;}$2Fe3O4+CO2;
②Fe3O4+CO$\frac{\underline{\;600-700℃\;}}{\;}$3FeO+CO2;
③FeO+O$\frac{\underline{\;>700℃\;}}{\;}$Fe+CO2
2铁的氧化物和硫酸铜溶液不反应,但都能与盐酸反应,其中除Fe2O3,为红棕色外,其余都为黑色,并且只有Fe3O4,能被磁铁吸引.
【猜想假设】小组同学一致认为黑色粉末一定是含有Fe的混合物,因为只有铁能和硫酸铜反应生成红色固体铜,并提出如下猜想:猜想1:黑色粉末是Fe和FeO,猜想2:黑色粉末是Fe和Fe3O4;猜想3:黑色粉末是Fe、FeO和Fe3O4.
【实验探究】小组同学经过思考、实验、合作和交流,最后得出猜想1成立的结论,下面是甲、乙两同学各自设计的一套验证猜想1的实验方案,请把表格补充完整.
| 实验操作 | 实验现象 | 实验结论 | 你对实验结论的评价(只需写出“对”或“错”) | |
| 甲 | 取适量黑色粉末于试管中,加入足量稀盐酸 | 黑色粉末完全溶解,并有气泡生成 | 猜想1正确 | 错 |
| 乙 | 取适量黑色粉末用磁铁吸引 | 黑色粉末部分被吸引 | 猜想1正确 | 错 |
| 实验操作 | 实验现象 | 实验现象 |
| 取适量黑色粉末用磁铁吸引 | 黑色粉末全部被吸引 | 猜想2正确 |
| 取适量黑色粉末用磁铁吸引,再向被吸引的黑色粉末中加入足量的硫酸铜溶液 | 黑色粉末部分被吸引,加入足量的硫酸铜溶液后黑色粉末仍然有剩余 | 猜想3正确 |
2.下列过程中不存在缓慢氧化的是( )
| A. | 生物的呼吸 | B. | 食物的腐败 | C. | 蜡烛缓慢地燃烧 | D. | 橡胶的老化 |
9.科学探究是奇妙的过程,请你一起参与实验探究.
(1)小松同学问用“双氧水”(过氧化氢溶液)清洗伤口时,不小心将过氧化氢溶液滴到水泥地板上,发现有大量气泡产生.小松联想到自己曾经用二氧化锰做过氧化氢的催化剂,他想,水泥块能否也可作过氧化氢分解的催化剂呢?于是他到附近建筑工地取回一些小水泥块,并用蒸馏水浸泡、冲洗、干燥,进行以下探究.
(2)【猜想】水泥块能做过氧化氢分解的催化剂.
(3)【实验论证】
(4)【结论】水泥块能加快过氧化氢的分解速率,故水泥块能做过氧化氢分解的催化剂.
(5)【讨论与反思】小芳认为:仅凭上述两个实验还不能证明水泥块为过氧化氢分解的催化剂,如觉得需要增加一个探究实验:探究水泥块在反应前后质量是否改变.
【实验步骤】a.准确称量水泥块的质量;b.完成实验二;c.待反应结束,将实验二试管里的物质进行过滤,洗涤、烘干、称量;d.对比反应前后水泥块质量.
【分析】如果水泥块反应前后质量不变,则说明水泥块可做过氧化氢分解的催化剂.
(6)但小华认为,要证明小松的猜想,小芳的补充实验还是不够的,需要再补充一个探究实验:
探究水泥块的化学性质在反应前后是否改变.
(1)小松同学问用“双氧水”(过氧化氢溶液)清洗伤口时,不小心将过氧化氢溶液滴到水泥地板上,发现有大量气泡产生.小松联想到自己曾经用二氧化锰做过氧化氢的催化剂,他想,水泥块能否也可作过氧化氢分解的催化剂呢?于是他到附近建筑工地取回一些小水泥块,并用蒸馏水浸泡、冲洗、干燥,进行以下探究.
(2)【猜想】水泥块能做过氧化氢分解的催化剂.
(3)【实验论证】
| 实验步骤 | 实验现象 | 实验结论 | |
| 试验一 | 常温下试管中加入过氧化氢溶液,然后伸入带火星的小木条 | 木条不复燃 | 常温下过氧化氢溶液不分解 |
| 实验二 | 在装有过氧化氢溶液的试管中加入水泥块,然后将带火星的木条伸入试管中 | 木条复燃 | 常温下水泥块能加快过氧化氢分解 |
(5)【讨论与反思】小芳认为:仅凭上述两个实验还不能证明水泥块为过氧化氢分解的催化剂,如觉得需要增加一个探究实验:探究水泥块在反应前后质量是否改变.
【实验步骤】a.准确称量水泥块的质量;b.完成实验二;c.待反应结束,将实验二试管里的物质进行过滤,洗涤、烘干、称量;d.对比反应前后水泥块质量.
【分析】如果水泥块反应前后质量不变,则说明水泥块可做过氧化氢分解的催化剂.
(6)但小华认为,要证明小松的猜想,小芳的补充实验还是不够的,需要再补充一个探究实验:
探究水泥块的化学性质在反应前后是否改变.
6.下边为甲(  )与乙(
)与乙(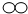 )反应生成丙(
)反应生成丙( )的粒子数变化示意图,
)的粒子数变化示意图,
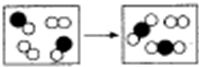
则下列说法正确的是( )
 )与乙(
)与乙(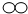 )反应生成丙(
)反应生成丙( )的粒子数变化示意图,
)的粒子数变化示意图,
则下列说法正确的是( )
| A. | 甲一定是氧化物 | B. | 如图的物质是纯净物 | ||
| C. | 该反应类型是分解反应 | D. | 该反应类型是化合反应 |