题目内容
4.“空气中氧气含量的测定”有多种方法.甲生设计了如图1如示的实验方案:在燃烧匙内盛过量红磷,点燃后立即插入集气瓶内,塞紧橡皮塞,待红磷火焰熄灭,集气瓶冷却至室温,打开铁夹,水注入集气瓶.回答下列问题: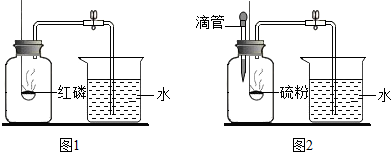
(1)反应结束后,打开铁夹,水自动注入集气瓶的直接原因是装置内的压强小于外界的气压
(2)乙生也设计了一个如图2所示的实验方案,装置和操作同甲类似,只不过用硫粉代替了红磷,并增加了滴管.要使实验成功,乙在滴管中应加入氢氧化钠溶液,可在反应后滴入,用于吸收燃烧产物,写出该溶液发生反应的化学方程式SO2+2NaOH=Na2SO3+H2O.(提示:生成物是亚硫酸钠和水.)
(3)丙生想利用氧气和某种金属的反应,来测定空气中的氧气含量.他选择利用下列仪器、药品:
(4)①带瓶塞的容积为V的烧瓶 ②电子天平(称量精度为0.01克)
③酒精灯 ④某种金属粉末.
他的实验步骤如下:准确称量某种金属粉末的质量M(足量),将其放入烧瓶,塞紧瓶塞,加热一段时间后(设金属不于其他气体反应),倒出烧瓶中粉末,并称其质量N(设氧气的密度为ρ).则氧含量为$\frac{N-M}{Vρ}$(用字母表示)
分析 (1)空气成分的测定实验的原理是利用某种物质燃烧消耗空气中某一成分,导致装置内的压强减小,从而使等体积液体倒流进入装置内.液体倒流的直接原因是装置内外的压强差,最根本的原因是物质燃烧对气体的消耗.这就要求生成物不能是气体,而当生成物为气体时,我们就必须想办法让液体能够和生成的气体反应或者溶解.
(2)乙同学实验中生成二氧化硫气体,借助二氧化硫的溶解性当然可以实现目的,但是为了促进溶解进行,或者叫启动反应的发生,我们可以借助更快捷的反应就是氢氧化钠溶液来吸收二氧化硫,这样水就能够更迅速进入装置内去溶解二氧化硫.
(4)对于使用天平来测定,要学会倒推,知道质量就可以根据密度求体积,所以要根据操作去分析实验的思路和原理.
解答 解:(1)空气成分的测定实验的原理是利用某种物质燃烧消耗空气中某一成分,导致装置内的压强减小,从而使等体积液体倒流进入装置内.液体倒流的直接原因是装置内外的压强差,最根本的原因是物质燃烧对气体的消耗.这就要求生成物不能是气体,而当生成物为气体时,我们就必须想办法让液体能够和生成的气体反应或者溶解.
(2)乙同学实验中生成二氧化硫气体,借助二氧化硫的溶解性当然可以实现目的,但是为了促进溶解进行,或者叫启动反应的发生,氢氧化钠溶液来吸收二氧化硫,这样水就能够更迅速进入装置内去溶解二氧化硫.
(4)根据题目中给定的天平和烧瓶体积的信息,可以称量金属在反应前后质量的变化,从而计算消耗的氧气的质量,根据氧气的密度求出氧气的体积,从而求出空气中氧气的含量.则氧含量为:$\frac{N-M}{ρ}÷V$=$\frac{N-M}{Vρ}$;
故答案:
(1)装置内的压强小于外界的气压;
(2)SO2+2NaOH=Na2SO3+H2O;
(4)$\frac{N-M}{Vρ}$.
点评 要在实验改进中学会根据实验的操作来研究实验的思路,例如本题在天平上就要结合题目中提供的操作过程去猜想实验思路.

| A. | 加碘盐 | B. | 蛋壳 | ||
| C. | 降温用的冰水混合体 | D. | 炒菜用的铁锅 |
【提出猜想】
钠能发生类似于CO2与镁的反应,可能的化学方程式为:4Na+CO2$\frac{\underline{\;点燃\;}}{\;}$2Na2O+C.
【进行实验】
将燃着的钠伸入装有CO2的集气瓶中,钠能在集气瓶中继续燃烧.
【查阅资料】得知:
①Na2O是白色固体,能与CO2反应生成Na2CO3,也能与H2O反应生成NaOH.
②Ba(OH)2溶于水而BaCO3不溶于水.
③Na2CO3的存在会干扰NaOH的检测.
基于以上资料,同学们认为钠在CO2中燃烧的产物情况有所不同,并对产物提出了以下几种猜想:
Ⅰ.Na2O、C;Ⅱ.Na2CO3、C;Ⅲ.NaOH、C;Ⅳ.Na2O、Na2CO3、C
通过理论分析,猜想Ⅲ(填序号)肯定错误的,理由是:NaOH中有氢元素而反应物中没有氢元素,根据质量守恒定律可知Ⅲ错误.
(三)【验证猜想】
| 步骤 | 实验操作 | 主要实验现象 | 结论(燃烧产物判断) |
| (1) | 将产物溶于适量水中 | 部分溶解,试管 底部有黑色固体 | 燃烧产物中肯定有C |
| (2) | 取少量(1)所得上层溶液,加入过量的 BaCl2溶液 | 有白色沉淀生成 | 燃烧产物中肯定有Na2CO3 |
| (3) | 取少量(2)所得上层溶液,加入CuSO4(或CuCl2)溶液 | 有蓝色沉淀生成 | 燃烧产物中肯定有Na2O |
【结论】
猜想Ⅳ(填序号)是正确的.
【交流】
步骤(3)中为检验第三种燃烧产物,也可以加入酚酞(或紫色石蕊试液、或能与OH-反应生成沉淀的可溶性物质)试剂.
| A. | 红磷在空气中燃烧后生成五氧化二磷固体 | |
| B. | 肥皂水滴入硬水中,产生较多泡沫,较少浮躁 | |
| C. | 硫在空气中燃烧发出淡蓝色火焰,产生有刺激性气味的气体 | |
| D. | 铁丝在空气中剧烈燃烧,火星四射,生成一种黑色固体 |
(1)对白色粉末成分的猜想和成因分析:经过反复思考,同学们认为白色粉末还可能是碳酸钙和氢氧化钙的混合物.
| 白色粉末的成分 | 形成的原因 |
| 可能是CaCO3 | 石灰水与空气中CO2反应; 化学方程式为:Ca(OH)2+CO2=CaCO3↓+H2O |
| 可能是Ca(OH)2 | 暑假气温较高,溶质的溶解度降低或溶剂蒸发,石灰水中的溶质结晶析出 |
| OH- | Cl- | CO32- | NO3- | |
| Ca2+ | 微 | 溶 | 不 | 溶 |
为了得出较严密的结论,他们进行了如下实验,请完成下列实验报告:
| 实验步骤 | 可能观察到的现象 | 结论 |
| 取上述试管中的上层清液,滴加1~2无色酚酞试液 | ||
| 往上述试管中的残留的固体中加入稀盐酸 | 白色粉末中有(选填“有”或“无”)CaCO3 | |
| 由上述实验可知白色粉末的成分是:Ca(OH)2、CaCO3. | ||
①通过上述实验的探究,同学们向实验室提出保存、使用易变质的溶液时的下列建议,合理的是AB(选填序号).
A.密封保存 B.使用前,临时配制 C.禁止使用这种试剂
②实验室清洗装石灰水试剂瓶内壁上的白色粉末时,可用稀盐酸,请写出其中可能发生的反应的化学方程式(写出一个即可):CaCO3+2HCl=CaCl2+CO2↑+H2O.