题目内容
18.在化学实验室,小刚和小强意外发现实验桌上有一瓶敞口放置的氢氧化钠固体,他们对这瓶氢氧化钠固体是否变质进行了如下实验探究:【提出问题】这瓶氢氧化钠固体是否变质?
【实验探究】为检验这瓶氢氧化钠固体是否变质,小刚和小强设计了如下实验方案:
小刚:取少量样品加适量蒸馏水配成溶液后,滴入几滴酚酞溶液,若观察到溶液变红色,证明该瓶氢氧化钠固体没有变质.
小强:取少量样品加适量蒸馏水配成溶液后,滴入适量澄清石灰水,若观察到有白色沉淀生成,证明该瓶氢氧化钠固体已经变质.
(1)你认为上述实验方案错误的是小刚:理由是碳酸钠溶液显碱性,也能使酚酞试液变红色.
请你设计另外一个方案,证明该瓶氢氧化钠固体已经变质,并完成以下实验报告:
| 实验步骤 | 实验现象及结论 |
| 取少量样品加适量蒸馏水配成溶液后,滴入适量氯化钙溶液 | 观察到有白色沉淀生成,证明该瓶氢氧化钠固体已经变质 |
分析 (1)氢氧化钠能和空气中的二氧化碳反应生成碳酸钠和水,氢氧化钠溶液和碳酸钠溶液都是显碱性的溶液,都能使酚酞试液变红色;
氢氧化钠不能和氯化钙反应,碳酸钠能和氯化钙反应生成白色沉淀碳酸钙和氯化钠;
(2)药品密封保存的原因很多,例如能够吸收空气中的水蒸气,能够和空气的某种物质发生反应,易挥发的药品都应该密封保存.
解答 解:(1)上述实验方案错误的是小刚,因为变质后的固体中含有碳酸钠,碳酸钠溶液显碱性,能使酚酞试液变红色.
故填:小刚;碳酸钠溶液显碱性,也能使酚酞试液变红色.
实验方案:取少量样品加适量蒸馏水配成溶液后,滴入适量氯化钙溶液,观察到有白色沉淀生成,这是因为氢氧化钠和二氧化碳反应生成了碳酸钠,碳酸钠和氯化钙反应生成了碳酸钙沉淀和氯化钠,实验过程如下表所示:
| 实验步骤 | 实验现象及结论 |
| 取少量样品加适量蒸馏水配成溶液后,滴入适量氯化钙溶液 | 观察到有白色沉淀生成,证明该瓶氢氧化钠固体已经变质 |
故填:浓硫酸能吸收水蒸气.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
6.某无色溶液中大量存在的离子如图所示,其中X可能是( )
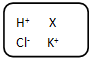

| A. | Ca2+ | B. | Fe3+ | C. | Na+ | D. | CO32- |
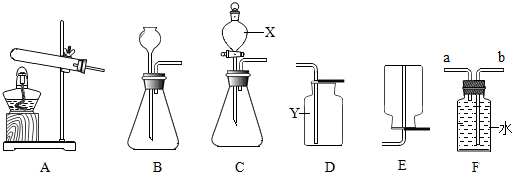
7.如图是某兴趣小组设计的四个实验装置,其中实验设计不正确的是( )
| A. |  蒸发食盐水 | B. |  测定空气中氧气的含量 | ||
| C. |  证明分子是不断运动的 | D. | 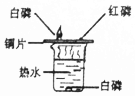 探究燃烧的条件 |
10. 碱式碳酸铜是一种难溶于水的绿色固体,受热易分解为氧化铜、水和二氧化碳.利用如图装置加热碱式碳酸铜一段时间,下列有关 描述正确的是( )
碱式碳酸铜是一种难溶于水的绿色固体,受热易分解为氧化铜、水和二氧化碳.利用如图装置加热碱式碳酸铜一段时间,下列有关 描述正确的是( )
 碱式碳酸铜是一种难溶于水的绿色固体,受热易分解为氧化铜、水和二氧化碳.利用如图装置加热碱式碳酸铜一段时间,下列有关 描述正确的是( )
碱式碳酸铜是一种难溶于水的绿色固体,受热易分解为氧化铜、水和二氧化碳.利用如图装置加热碱式碳酸铜一段时间,下列有关 描述正确的是( )| A. | 试管口有水珠生成 | |
| B. | 试管内的固体由绿色变为红色 | |
| C. | 烧杯内盛放 NaOH 溶液检验生成的 CO2 | |
| D. | 实验结束后应先停止加热,后将导管移出烧杯 |
8.下列有关水的说法中正确的是( )
| A. | 水的蒸发和水通电分解都属于物理变化 | |
| B. | 硬水和软水可用石蕊溶液来区分 | |
| C. | 硬水是指含有较多可溶性钙、镁化合物的水 | |
| D. | 有水生成的反应一定是酸和碱的中和反应 |