题目内容
12.乙烯(C2H4)是石油炼制的重要产物之一.常温常压时,乙烯是一种气体,它与另一种气体组成的混合物中碳元素的质量分数为85%,则另一种气体不可能是( )| A. | H2 | B. | CH4 | C. | CO | D. | C2H2 |
分析 根据物质中某元素的质量分数=$\frac{该元素的相对原子质量\;\;×\;\;\;原子个数\;\;\;\;\;}{化合物的相对分子质量}$×100%,先计算出乙烯中碳元素的质量百分比为 85.7%,因为,混合气体的碳元素质量分数为85%,而乙烯>85%,所以,另一种气体的含碳量一定要<85%才能是混合气体中碳元素质量分数等于85%,分别计算出选项中碳元素的质量百分比,即可解答.
解答 解:乙烯中,碳元素的质量百分比=$\frac{12×2}{12×2+4}$×100%=85.7%,
A、H2中不含有碳元素,碳元素的质量百分比为0;
B、CH4中碳元素的质量百分比=$\frac{12}{16}$×100%=75%;
C、CO中碳元素的质量百分比=$\frac{12}{12+16}$×100%=42.9%;
D、C2H2中碳元素的质量百分比=$\frac{12×2}{12×2+2}$×100%=92.3%;
因为,混合气体的碳元素质量分数为85%,而乙烯>85%,所以,另一种气体的含碳量一定要小于85% 才能使混合气体中碳元素质量分数等于85%;
故选D.
点评 本题考查学生利用质量分数与混合物中元素的质量分数进行比较进行分析解题的能力.

练习册系列答案
相关题目
2.李明同学对蜡烛及其燃烧进行了探究.按要求填写下列实验现象及其结论.
结论:蜡烛燃烧生成水和二氧化碳.
提出问题:蜡烛在刚熄灭时,总会有一缕白烟冒出,白烟的成分是③.
①白烟是蜡烛燃烧时生成的二氧化碳
②白烟是蜡烛燃烧时生成的水蒸气
③白烟是石蜡蒸气凝结成的石蜡固体小颗粒.
| 探究步骤 | 对实驗的观察和描述 |
| 点燃前 | 石蜡放入水中观察到的现象是石蜡浮在水面上,难溶于水 |
| 燃着时 | ①点燃蜡烛,把一根火柴梗放在蜡烛的火焰中,约1s后取出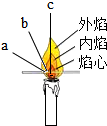 可以看到火柴梗的a(选填图中字母)处最先炭化,说明此处温度最高. |②在火焰上方罩一个干冷的烧杯,一会儿后•烧杯内壁出现水珠现象,倒入澄清石灰水,现象为石灰水变浑浊. |
| 熄灭后 | 吹灭蜡烛,观察到一缕白烟. |
提出问题:蜡烛在刚熄灭时,总会有一缕白烟冒出,白烟的成分是③.
①白烟是蜡烛燃烧时生成的二氧化碳
②白烟是蜡烛燃烧时生成的水蒸气
③白烟是石蜡蒸气凝结成的石蜡固体小颗粒.
7.日常生活中见到下列现象,其中只发生了物理变化的是( )
| A. | 鞭炮爆炸 | B. | 轮胎爆裂 | C. | 鸡蛋变臭 | D. | 植物生长 |
17.走进实验室,我们学会了科学探究的最基本的操作,以下实验操作正确的是( )
| A. | 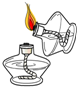 点燃酒精灯 | B. |  闻药品的气味 | C. | 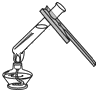 加热液体 | D. | 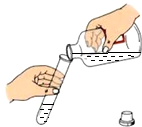 倾倒液体 |
2.某试剂敞口放置在空气中一段时间后,溶质质量分数会变小,但溶液质量会变大且溶质成分不变,则该试剂可能是( )
| A. | 浓盐酸 | B. | 浓硫酸 | C. | 食盐水 | D. | 石灰水 |