题目内容
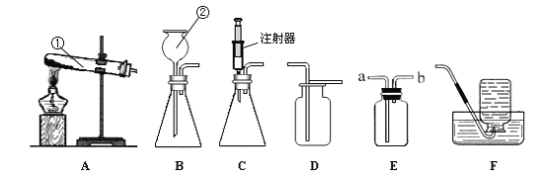
【题目】用下图所示实验验证质量守恒定律。
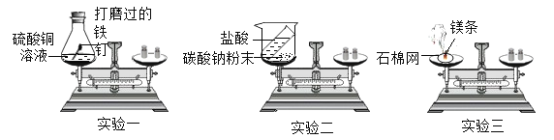
(1)实验一中,将铁钉浸到硫酸铜溶液中,发生反应的化学方程式为______。观察到的现象是______,成功验证质量守恒定律。
(2)实验二中,反应前后天平不平衡,用文字结合化学方程式解释其原因______。
(3)实验三中,称量镁条和石棉网的质量后,点燃镁条,观察到______,再称量指针指在刻度盘中央,无法验证质量守恒定律。该反应的化学方程式为______。
【答案】Fe+CuSO4═FeSO4+Cu 铁钉表面出现红色固体,溶液由蓝色变成浅绿色 Na2CO3+2HCl═2NaCl+H2O+CO2↑,生成的二氧化碳逸出装置 镁条燃烧,发出耀眼的白光,放热,生成白色固体 2Mg+O2![]() 2MgO
2MgO
【解析】
(1)将铁钉浸到硫酸铜溶液中,铁和硫酸铜反应生成硫酸亚铁和铜,发生反应的化学方程式为:Fe+CuSO4═FeSO4+Cu,观察到铁钉表面出现红色固体,溶液由蓝色变成浅绿色;
(2)实验二中,反应前后天平不平衡,其原因:盐酸和碳酸钠反应生成氯化钠、水和二氧化碳,反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑,生成的二氧化碳逸出装置;
(3)实验三中,称量镁条和石棉网的质量后,点燃镁条,观察到镁条燃烧,发出耀眼的白光,放热,生成白色固体,该反应的化学方程式为:2Mg+O2![]() 2MgO。
2MgO。

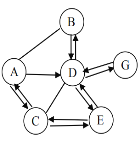
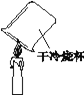
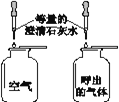
【题目】根据下图所示的验证实验进行分析,得出的结论不正确的是
|
|
|
|
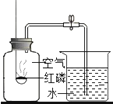
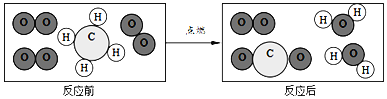
A.黄铜比纯铜 硬度大 | B.蜡烛中含有氢、氧元素 | C.呼出的气体中二氧化碳含量比空气高 | D.分子在不断地运动 |
A. A B. B C. C D. D
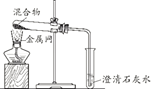
【题目】为探究碳还原氧化铜的最佳实验条件,用木炭粉和氧化铜的干燥混合物1~2.5 g进行系列实验。
(查阅资料)
①氧化铜(CuO)为黑色固体。铜不与稀硫酸反应。
②碳还原氧化铜得到的铜中可能含有少量的氧化亚铜;氧化亚铜为红色固体,能与稀硫酸反应:Cu2O + H2SO4 ==== CuSO4 + Cu + H2O
(进行实验)
实验1:取质量比为1:11的木炭粉和氧化铜混合物1.3 g,进行实验。
序号 | 1-1 | 1-2 |
装置 |
|
|
反应后物质的颜色、状态 | 黑色粉末中混有少量红色固体 | 红色固体有金属光泽,混有极少量黑色物质 |
实验2:取一定质量的混合物,用1-2装置进行实验。
序号 | 木炭粉与氧化铜的质量比 | 反应后物质的颜色、状态 | |
2-1 | 1:9 | 红色固体有金属光泽 | 混有少量黑色物质 |
2-2 | 1:10 | 混有很少量黑色物质 | |
2-3 | 1:11 | 混有极少量黑色物质 | |
2-4 | 1:12 | 无黑色物质 | |
2-5 | 1:13 | 混有较多黑色物质 | |
(解释与结论)
(1)配平化学方程式:___C +__CuO![]() __Cu +__CO2↑
__Cu +__CO2↑
(2)实验1-2中,证明产生了CO2的现象是_______。
(3)实验1的目的是_______。
(4)实验2的结论是_______。
(反思与评价)
(5)实验2没有进行质量比为1:14的实验,理由是_______。
(6)为检验2-4的红色固体中是否含Cu2O,所需试剂是_______。
【题目】下列关于化学实验的“目的-操作-现象-结论”的描述正确的是( )
实验目的 | 操作 | 实验现象 | 实验结论 | |
A | 检验稀盐酸和氢氧化钠溶液是否恰好完全反应 | 在反应后的溶液中滴加无色酚酞试液 | 无明显现象 | 恰好完全反应 |
B | 判断海水和蒸馏水 | 蒸发结晶 | 液体消失,无残留物 | 该液体为蒸馏水 |
C | 检验溶液中是否含硫酸根离子 | 加入氯化钡溶液,再加入稀硝酸 | 有白色沉淀产生 | 溶液中一定含硫酸根离子 |
D | 测定空气中氧气的体积分数 |
| 红磷燃烧,产生大量白色烟雾;完全燃烧后,立即打开弹簧夹,进入水的体积约为集气瓶总体积的五分之一 | 氧气约占空气体积的五分之一 |
A. A B. B C. C D. D