题目内容
10. 如图是甲、乙、丙三种固体物质的溶解度曲线,请回答下列问题:
如图是甲、乙、丙三种固体物质的溶解度曲线,请回答下列问题:(1)A点的含义是t2℃时,甲、乙、丙物质的溶解度相等;
(2)t2℃时,将25 g乙加入到50 g水中,充分溶解,所得溶液 中溶质与溶液的质量比是2:7;
(3)t3℃时,在等质量的甲、乙、丙三种物质饱和溶液中,含剂最多的是丙(填“甲”、“乙”或“丙”);
(4)若要将组成在N点的丙溶液转化为M点的丙溶液,可采用 的方法是增加溶剂;
(5)t1℃时,将甲、乙、丙三种物质的饱和溶液升温到t3℃,所得溶液的溶质质量分数 由小到大的顺序是甲<丙<乙.
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)通过分析溶解度曲线可知,A点的含义是:t2℃时,甲、乙、丙物质的溶解度相等;
(2)t2℃时,乙物质的溶解度是40g,所以将25g乙加入到50g水中,充分溶解,所得溶液中溶质与溶液的质量比是:20g:70g=2:7;
(3)t3℃时,丙物质的溶解度最小,所以在等质量的甲、乙、丙三种物质饱和溶液中,含剂最多的是丙;
(4)若要将组成在N点的丙溶液转化为M点的丙溶液,温度不变,溶液由饱和变成不饱和,可采用的方法是增加溶剂;
(5)t1℃时,乙物质的溶解度大于甲物质的溶解度,升高温度,甲、乙物质不会析出晶体,丙物质会析出晶体,应该按照t3℃时的溶解度进行计算,所以所以t1℃时,将甲、乙、丙三种物质的饱和溶液升温到t3℃,所得溶液的溶质质量分数由小到大的顺序是甲<丙<乙.
故答案为:(1)t2℃时,甲、乙、丙物质的溶解度相等;
(2)2:7;
(3)丙;
(4)增加溶剂;
(5)甲<丙<乙.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
相关题目
20.下列除杂质所选用的试剂及实验操作均正确的是( )
| 选项 | 物质(括号内为杂质) | 除杂试剂 | 实验操作 |
| A | KCl(KOH) | 稀 H2SO4 | 蒸发结晶 |
| B | CO2(CO) | O2 | 点燃 |
| C | MnO2(KClO3) | 水 | 溶解、过滤 |
| D | 铁粉(碳粉) | 稀 HCl | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
1.“生活离不开化学”,下列叙述合理的是( )
| A. | 食用加碘盐可以预防大脖子病,所以应尽量多吃 | |
| B. | 煤、石油、天然气都是不可再生能源 | |
| C. | 用甲醛溶液浸泡鱿鱼,以保质保鲜 | |
| D. | 有人称自己有特异功能,能“化水为油” |
5.分析推理是一种重要的化学思维方法.下列推理正确的是( )
| A. | 分子、原子可以构成物质,所以物质一定是由分子、原子构成的 | |
| B. | 碱性溶液能使酚酞试液变红色,所以能使酚酞试液变红色的溶液的pH一定大于7 | |
| C. | 溶液的特征是均一、稳定,所以均一、稳定的液体一定是溶液 | |
| D. | 稀有气体元素的原子最外层有8个(氦是2个)电子,所以微粒 一定是稀有气体元素的原子 一定是稀有气体元素的原子 |
2.甲组同学往20克10%的氢氧化钠溶液样品中滴加10% 的盐酸(室温下).如图描述的是氢氧化钠与盐酸反应的微观实质.
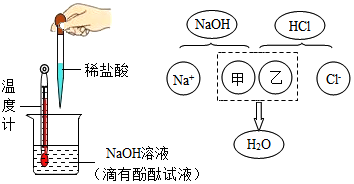
(1)从分类角度:氢氧化钠属于C.
A、氧化物 B、酸 C、碱 D、盐
(2)从宏观与微观角度:
?请从微观的角度分析,甲、乙处应填入的化学符号依次是OH-、H+.
请用离子符号表示酸碱中和反应的本质:OH-+H+=H2O.
?判断在盐酸溶液中一定能大量共存的离子组是D
A、Na+、K+、CO32- B、Ag+、NO3-、SO42-
C、Cu2+、NO3-、OH- D、K+、NH4+、SO42-
(3)从能量角度
反应中溶液温度的变化 记录如表,据表数据分析:
①当加入盐酸体积为6mL时,表明NaOH与HCl恰好完全反应.此判断的依据是此时温度上升最高.
②当加入4mL盐酸时,烧杯中溶液仍然呈红色,该溶液中含有的溶质有酚酞和NaCl、NaOH.(写化学式)

(1)从分类角度:氢氧化钠属于C.
A、氧化物 B、酸 C、碱 D、盐
(2)从宏观与微观角度:
?请从微观的角度分析,甲、乙处应填入的化学符号依次是OH-、H+.
请用离子符号表示酸碱中和反应的本质:OH-+H+=H2O.
?判断在盐酸溶液中一定能大量共存的离子组是D
A、Na+、K+、CO32- B、Ag+、NO3-、SO42-
C、Cu2+、NO3-、OH- D、K+、NH4+、SO42-
| 加入盐酸的体积(V)/mL | 2 | 4 | 6 | 8 | 10 |
| 溶液温度上升(△t)/℃ | 5.6 | 12.1 | 18.5 | 15.2 | 13.5 |
反应中溶液温度的变化 记录如表,据表数据分析:
①当加入盐酸体积为6mL时,表明NaOH与HCl恰好完全反应.此判断的依据是此时温度上升最高.
②当加入4mL盐酸时,烧杯中溶液仍然呈红色,该溶液中含有的溶质有酚酞和NaCl、NaOH.(写化学式)
9.下列溶液中,pH大于7的是( )
| A. | 稀氢氧化钠溶液 | B. | 稀盐酸 | C. | 氯化钠溶液 | D. | 稀硫酸 |
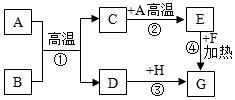 A~H是初中化学常见的物质,已知A为黑色固体单质,G为紫红色固体单质,B为红棕色粉末,H为蓝色的硫酸盐溶液.它们的转化关系如图所示,回答问题:
A~H是初中化学常见的物质,已知A为黑色固体单质,G为紫红色固体单质,B为红棕色粉末,H为蓝色的硫酸盐溶液.它们的转化关系如图所示,回答问题: