题目内容
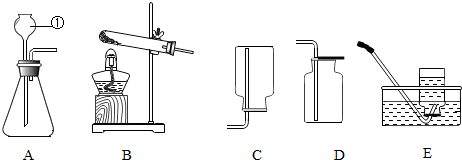
17.某校化学兴趣小组经查阅资料得知:尽管铝表面致密的氧化膜能使铝与其周围的介质(空气、水)隔绝,但“奇怪”的是铝制容器仍不能用来盛放和腌制咸菜.为此该小组对铝的氧化膜进行了探究实验,其过程如下,请完成填空:【实验1】用坩埚钳夹住一块擦去氧化膜的铝片,放在酒精灯火焰上灼烧,铝片表面接触火焰的部分变暗片刻后变软;轻轻摇动,会左右摇晃,却不像蜡烛那样滴落.在空气中灼烧铝片会生成Al2O3(填化学式);
【实验2】取2条未用砂纸打磨过的铝片,A片浸入CuCl2稀溶液中,其表面很快析出较多红色粉末状固体;而另B片浸入CuSO4稀溶液中无明显反应现象.
进行猜测与猜测:氯离子可能会对铝表面的氧化膜产生破坏作用.
【实验3】另取用砂纸打磨的一片铝片使其表面较粗糙,将其放入另一CuSO4稀溶液中,直到2-3分钟后,铝片表面才有少量红色固体附着.该反应属于置换基本反应类型.
【实验4】向实验2的CuSO4稀溶液中滴入3-5滴NaCl稀溶液,铝片表面逐渐有红色固体析出.称量实验反应前后的B片铝片(取出并擦干净),金属片的质量变大(填“变大”“变小”或“不变”)(Al-27 Cu-64)
【实验5】向实验2的CuSO4稀溶液中滴3-5滴Na2SO4稀溶液,铝片表面现象一直不明显.
根据实验2、3、4、5的现象可以得出的结论是氯离子对铝和氯化铜溶液的反应有促进作用;硫酸根离子对铝和硫酸铜溶液的反应有抑制作用.
分析 【实验1】
灼烧时,铝能和空气中的氧气反应生成氧化铝;
【实验2】
根据实验现象可以判断实验结论;
【实验3】
一种单质和一种化合物反应生成另一种单质和另一种化合物的反应属于置换反应;
【实验4】
铝和硫酸铜反应生成硫酸铝和铜,根据反应的化学方程式及其反应物和生成物的质量关系可以进行相关方面的判断;
【实验5】根据实验现象可以判断实验结论.
解答 解:【实验1】
灼烧时,铝能和空气中的氧气反应生成氧化铝,氧化铝的化学式是Al2O3.
故填:Al2O3.
【实验2】
取2条未用砂纸打磨过的铝片,A片浸入CuCl2稀溶液中,其表面很快析出较多红色粉末状固体;而另B片浸入CuSO4稀溶液中无明显反应现象,说明氯离子可能会对铝表面的氧化膜产生破坏作用.
故填:氯.
【实验3】
铝和硫酸铜反应生成硫酸铝和铜,属于置换反应.
故填:置换.
【实验4】
铝和硫酸铜反应的化学方程式及其反应物、生成物的质量关系为:2Al+3CuSO4═Al2(SO4)3+3Cu,
54 192
由质量关系可知,反应了54份质量的铝时,会有192份质量的铜附着在铝片上,因此称量实验反应前后的B片铝片时,金属片的质量变大.
故填:变大.
【实验5】
根据实验2、3、4、5的现象可以得出的结论是氯离子对铝和氯化铜溶液的反应有促进作用;硫酸根离子对铝和硫酸铜溶液的反应有抑制作用.
故填:氯离子对铝和氯化铜溶液的反应有促进作用;硫酸根离子对铝和硫酸铜溶液的反应有抑制作用.
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

练习册系列答案
相关题目
5.如表所示除去杂质的方法中,错误的是( )
| 选项 | 物质 | 杂质 | 除杂质的方法 |
| A. | 稀硫酸 | 铜 | 过滤 |
| B. | CaSO4溶液 | 稀硫酸 | 过量CaCO3、过滤 |
| C. | FeCl2溶液 | CuCl2 | 过量铁粉、过滤 |
| D. | 二氧化碳 | 一氧化碳 | 点燃 |
| A. | A | B. | B | C. | C | D. | D |

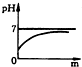
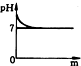
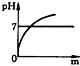
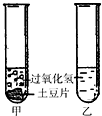 小明将一片土豆放入过氧化氢溶液中,发现过氧化氢溶液的分解速率加快.查阅资料后知道土豆中含有一种生物催化剂--过氧化氢酶,于是他设计了如下实验:常温下将几片土豆放入甲试管,分别往甲、乙试管内注入相同体积与溶质质量分数的过氧化氢溶液(如图所示),观察试管内气泡产生的速率.
小明将一片土豆放入过氧化氢溶液中,发现过氧化氢溶液的分解速率加快.查阅资料后知道土豆中含有一种生物催化剂--过氧化氢酶,于是他设计了如下实验:常温下将几片土豆放入甲试管,分别往甲、乙试管内注入相同体积与溶质质量分数的过氧化氢溶液(如图所示),观察试管内气泡产生的速率.