题目内容
8. 如图为某物质的分子模型示意图,其中“
如图为某物质的分子模型示意图,其中“ ”代表氢原子,“
”代表氢原子,“ ”代表氧原子.下列有关叙述不正确的是( )
”代表氧原子.下列有关叙述不正确的是( )| A. | 此物质属于化合物 | B. | 此物质中氧元素的化合价为-2价 | ||
| C. | 此物质的一个分子由4个原子构成 | D. | 此物质中氢氧元素的质量比是1:16 |
分析 先根据模型图写出化学式,然后根据化学式进行计算或判断,纯净物中各元素的质量比等于相对原子质量和的比.
解答 解:由物质的分子模型示意图,该物质的每个分子由2个H原子和2个O原子构成,则物质的化学式为H2O2.
A.H2O2是由两种元素组成的纯净物,属于化合物,故正确;
B.在H2O2中,氢元素显+1价,设其中氧元素的化合价为x,则(+1)×2+2x=0,x=-1,故错误;
C.由物质的分子模型示意图,该物质的一个分子由2个H原子和2个O原子共4个原子构成,故正确;
D.该物质的化学式为H2O2,其中H、O元素质量比=(1×2):(16×2)=1:16;故正确.
故选B.
点评 辨认分子结构模拟图是解答此类问题的基础,由分子结构模拟图推断出物质的化学式则是解答本题的一种方法.

练习册系列答案
相关题目
16.如图所示为a、b两种物质的 溶解度曲线,则下列说法错误的是( )
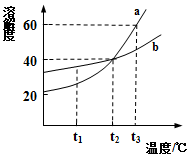

| A. | a、b的溶解度都随温度的升高而增大 | |
| B. | t1℃时,b的溶解度大于a的溶解度 | |
| C. | t2℃时,a、b的溶解度相同,均为40克 | |
| D. | t3℃时,a的饱和溶液中溶质的质量分数为60% |
3.氯化钠是工业生产和生活的一种重要原料,也是实验室里常见的一种药品.下表是20℃时,氯化钠溶解于水的实验数据,回答下列问题;
(1)计算第1次实验得到的氯化钠溶液的溶质质量分数.
(2)m=13.6;
(3)在这4次实验中,得到的氯化钠溶液属于饱和溶液的是③④(填实验序号)
(4)20℃时,实验室把100克溶质质量分数为20%的氯化钠溶液释成5%的氯化钠溶液,需加水多少毫升?
| 实验序号 | 水的质量(g) | 加入氯化钠的质量(g) | 溶液的质量(g) |
| ① | 10 | 2 | 12 |
| ② | 10 | 3 | 13 |
| ③ | 10 | 4 | 13.6 |
| ④ | 10 | 5 | m |
(2)m=13.6;
(3)在这4次实验中,得到的氯化钠溶液属于饱和溶液的是③④(填实验序号)
(4)20℃时,实验室把100克溶质质量分数为20%的氯化钠溶液释成5%的氯化钠溶液,需加水多少毫升?
13.电解水实验中,其中一极产生氢气6cm3,则另一极产生的氧气体积应为( )
| A. | 12cm3 | B. | 6cm3 | C. | 3cm3 | D. | 2cm3 |
17.下列说法不正确的是( )
| A. | 一切物质的化学性质都是在化学变化中表现出来的 | |
| B. | 铁合金、铜合金、铝合金不是纯净物 | |
| C. | 烧碱在水中电离出氢氧离子和钠离子,其水溶液呈电中性和碱性 | |
| D. | 加到水里的生石灰在反应前后质量和化学性质均不变 |
18.“厨房化学”是指利用家庭生活用品拿来进行生活实验,有利于对化学进行探究活动.下列实验能在“厨房化学”中完成的是( )
| A. | 检验食盐中是否含有氯元素 | B. | 检验自来水是否用氯气消毒 | ||
| C. | 检验鸡蛋壳是否可溶于酸 | D. | 确定味精的元素组成 |
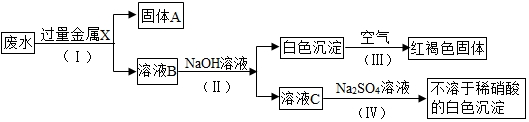
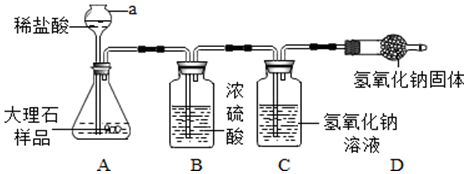
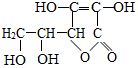 黄瓜中富含维生素C,其分子结构如图.维生素c的化学式C6H8O6.维生素C在pH<5的环境中较稳定,为减少维生素C的损失,黄瓜在烹饪时应加入少量的食醋.维生素C片保存时,应注意避热、避光、密封,请你据此推测维生素c的化学性质受热易分解或者见光易分解(合理即可).
黄瓜中富含维生素C,其分子结构如图.维生素c的化学式C6H8O6.维生素C在pH<5的环境中较稳定,为减少维生素C的损失,黄瓜在烹饪时应加入少量的食醋.维生素C片保存时,应注意避热、避光、密封,请你据此推测维生素c的化学性质受热易分解或者见光易分解(合理即可).