题目内容
化学学科的特征是在原子、分子水平上研究物质和创造物质.
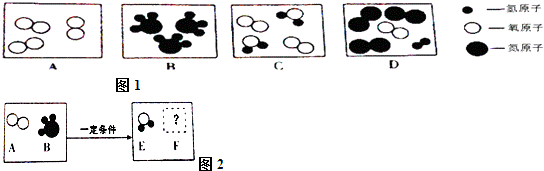
(1)请从微观的角度解释:金属Na、Mg性质不同的原因是 ;CO和CO2性质不同的原因是 ;
(2)A、B、C、D四种物质的微观示意图如图1所示:
①从微观的角度看,B图表示: ,(填化学符号).
②从宏观角度看,图中表示混合物的是 (填字母编号).
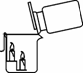
(3)在一定条件下,A和B能发生化学反应生成E和F,其微观示意图如图2所示
①若F为空气中体积分数最大的气体,写出该反应的化学方程式: .
②一定条件下,若A、B和E的分子个数比为5:4:6,则F的化学式为 .
答案 分析:
(1)根据已有的知识进行分,元素的化学性质与原子最外层电子数有关,物质的构成不同则性质不同,据此解答.
(2)①根据物质的微观构成,写出化学符号;
②根据物质的微观构成分析物质的类别;
(3)根据微观示意图和空气的成分,分析反应物、生成物.写出化学式及反应的方程式.
解:(1)金属Na、Mg性质不同的原因是最外层电子数不同;一氧化碳和二氧化碳性质不同的原因是二者的分子构成不同;故填:原子结构不同(或最外层电子数不同);分子结构不同(其他合理答案均可);
(2)①由物质的微观构成,B图中有三个构成相同的分子,每个分子是由三个氢原子和一个氮原子构成所以,B图表示:3NH3;
②由物质的微观构成可知,CD都是由不同种分子构成的物质,宏观上是由不同种物质组成的,属于混合物;
(3)根据“A和B能发生化学反应生成E和F”,由微观示意图和可知:
①A是氧气、B是氨气,C是水,F为空气中体积分数最大的气体,则F是氮气,则该反应的化学方程式为:4NH3+3O2 6H2O+2N2;
6H2O+2N2;
②一定条件下,若A、B和E的分子个数比为5:4:6,则可推测反应的化学方程式为:4NH3+5O2 6H2O+4NO,则F的化学式为NO.
6H2O+4NO,则F的化学式为NO.
故答案为:
(1)原子结构不同(或最外层电子数不同);分子结构不同(其他合理答案均可)
(2)①NH3; ②C; D;
(3)①4NH3+3O2 6H2O+2N2;②NO
6H2O+2N2;②NO

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案某学校课外活动小组,对本地化工厂排放废水中的盐酸含量进行了测定.取废水50g,用2%的氢氧化钠溶液进行中和,当溶液pH=7时,用去氢氧化钠溶液20g.计算废水中盐酸的溶质质量分数.
测定时,有同学发现在反应过程中,溶液有温度的变化,于是他们进一步进行了探究.
(1)配制100mL10%的盐酸(密度为1.05g/cm3).他们应量取38%的盐酸(密度为1.19g/cm3)多少毫升?
(2)在一定体积的10%的氢氧化钠溶液中,慢慢滴入上述配制的10%的盐酸.有关实验中的数据记录如下:
| 加入盐酸的体积(V)/mL | 2 | 4 | 6 | 8 | 10 |
| 溶液温度变化(△t)/℃ | 5.2 | 9.6 | 13.0 | 16.0 | 18.2 |
试在如图坐标系中绘出溶液温度变化与加入盐酸体积之间的变化关系图.
(3)根据(2)中关系图,请你从能量变化的角度谈谈对中和反应的认识.

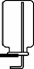
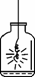
 ;
; 于室内 排放不畅引起的;
于室内 排放不畅引起的;
