题目内容
7.现有如图1所示装置、仪器.请根据要求回答问题: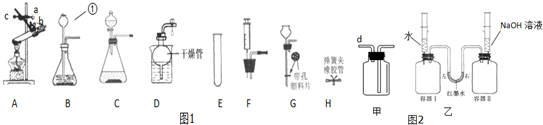
(1)仪器①的名称是长颈漏斗.
(2)图A是实验室用高锰酸钾制取氧气的装置,为使试管口略向下倾斜,应该调节的螺丝是c(选填“a”、“b”或“c”),装置改正后试管中发生反应的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑.
(3)实验室用过氧化氢溶液分解制取O2,若要控制反应速率获得平稳气流,应选用C(从A至D选填序号)作为气体发生装置.
(4)若用如图2甲除去CO中的CO2,瓶中装入的试剂最好是①(选填数字:①烧碱溶液 ②浓硫酸
③澄清石灰水),气体从e(选填“d”或“e”)通入.
(5)如图2乙装置中容器Ⅰ、Ⅱ都盛等体积CO2,分别用注射器向两个容器中注入等量的水和NaOH溶液,观察到U形管中右边液面上升(或U形管中左边液面下降)现象,说明CO2能与NaOH溶液发生反应,写出反应的化学方程式CO2+2NaOH═Na2CO3+H2O.
分析 (1)根据仪器名称解答;
(2)根据装置的特点和加热高锰酸钾制取氧气的反应原理解答;
(3)C装置通过控制分液漏斗的活塞,可以控制反应的速度;
(4)由于氢氧化钠是极易溶于水的故溶液中的溶质多能保证把二氧化碳充分吸收,故用如图甲除去CO中的CO2,瓶中装入的试剂最好是:①.烧碱溶液;
(5)根据氢氧化钠溶液比水吸收的二氧化碳多来解答.
解答 解:(1)仪器①的名称是长颈漏斗;
(2)使试管口略向下倾斜,应该调节的螺丝是c,用高锰酸钾制取氧气的化学方程式是:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)C装置通过控制分液漏斗的活塞,可以控制反应的速度;若要控制反应速率获得平稳气流,应选用C作为气体发生装置.
(4)由于氢氧化钠是极易溶于水的故溶液中的溶质多能保证把二氧化碳充分吸收,故用如图甲除去CO中的CO2,瓶中装入的试剂最好是:①.烧碱溶液;
(5)氢氧化钠溶液比水吸收的二氧化碳多,故容器Ⅱ压强小于容器Ⅰ,故观察U形管中右边液面上升现象时,说明CO2能与NaOH溶液发生反应.氢氧化钠溶液吸收二氧化碳生成碳酸钠和水,反应的化学方程式是CO2+2NaOH═Na2CO3+H2O.
答案:
(1)长颈漏斗;
(2)c; 2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;
(3)C;
(4)①;e;
(5)U形管中右边液面上升(或U形管中左边液面下降);CO2+2NaOH═Na2CO3+H2O.
点评 本题主要考查的是常用气体的发生装置和收集装置的选取方法,要熟记常用气体的发生装置和收集装置与选取方法及其依据,还有氧气、二氧化碳的实验室制取方法,有时还需弄清图示信息等等.

| A. | 百炼成钢 | B. | 钢铁生锈 | ||
| C. | 石油分馏 | D. | 蛋白质遇浓硝酸呈黄色 |
| A. | 生石灰粉 | B. | 熟石灰 | C. | 炭粉 | D. | 铁粉 |
| A. | 室温下pH值<7的溶液呈酸性,所以pH值<7的雨水是酸雨 | |
| B. | 有机物中都含碳元素,所以含碳元素的化合物都是有机物 | |
| C. | 金刚石和石墨都是由碳原子构成,所以它们的性质相同 | |
| D. | 碱性溶液能使石蕊试液变蓝,所以能使石蕊试液变蓝的溶液一定呈碱性 |
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 所取合金的质量∕g | 10 | 10 | 20 | 30 |
| 所加稀硫酸的质量∕g | 100 | 120 | 80 | X |
| 生成氢气的质量∕g | 0.2 | 0.2 | 0.2 | Y |
(1)上表第四次实验中合金里的铁恰好与稀硫酸完全反应,则X=240Y=0.6;
(2)所加稀硫酸溶质质量分数为多少?(结果保留至0.1%).
