题目内容
5.人类的生活和生产都离不开金属材料.(1)下列物品中,利用金属导热性的是A(填字母序号).

(2)中国是自行车大国.钢材是使用在自行车上最久的车架材质,钢的缺点是易生锈,生锈的原因是铁与氧气和水反应的结果.
(3)工业上,用一氧化碳和赤铁矿炼铁的化学方程式是3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
分析 (1)根据金属具有良好的导电性、导热性和延展性等解答;
(2)根据铁生锈的条件解答;
(3)根据高温条件下,一氧化碳和氧化铁反应生成铁和二氧化碳解答.
解答 解:(1)铁用作铁锅,是利用了铁具有良好的导热性.
故选:A.
(2)钢材是使用在自行车上最久的车架材质,钢的缺点是易生锈,生锈的原因是铁与氧气和水反应的结果.
(3)高温条件下,一氧化碳和氧化铁反应的化学方程式为:Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2.
答案:(1)A;(2)氧气和水; (3)3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2
点评 物质的结构决定物质的性质,物质的性质决定物质的用途,要注意掌握.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案
相关题目
16. 南南同学看到“好想你”红枣袋中装有一袋防腐剂,品名为
南南同学看到“好想你”红枣袋中装有一袋防腐剂,品名为
“504双吸剂”,其标签如图所示.南南和北北对这包久置的“504双吸剂”
固体样品很好奇,设计如下实验进行探究.
【提出问题】久置固体的成分是什么?
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁.
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.
【实验探究】
南南同学的方案
北北同学认为南南同学的实验并不能得出一定不含Fe2O3的结论,理由是氧化铁和盐酸反应生成氯化铁,铁和氯化铁反应生成氯化亚铁,溶液也是浅绿色,并设计如下实验方案继续验证.
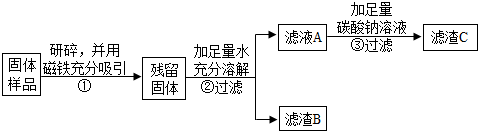
(1)步骤①样品用磁铁吸引前需经过研碎,其中研碎的目的是增大接触面积,使反应充分.
(2)步骤②中固体溶解时放出大量热,由此可以判断固体中一定含有CaO.写出该过程中的化学方程式CaO+H2O=Ca(OH)2.
(3)步骤③中反应的化学方程式是Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
北北同学对滤渣B又进行探究.
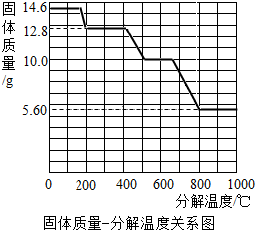
【实验结论】综合上述实验及所给数据,该久置固体中一定含有的物质是Fe、Fe2O3、CaO、CaCO3.
 南南同学看到“好想你”红枣袋中装有一袋防腐剂,品名为
南南同学看到“好想你”红枣袋中装有一袋防腐剂,品名为“504双吸剂”,其标签如图所示.南南和北北对这包久置的“504双吸剂”
固体样品很好奇,设计如下实验进行探究.
【提出问题】久置固体的成分是什么?
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁.
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.
【实验探究】
南南同学的方案
| 实验操作 | 实验现象 | 实验结论 |
| 取少量固体放于试管中,滴加足量的稀盐酸 | 固体逐渐消失,有无色气体产生,得到浅绿色溶液 | 固体有一定含有Fe, 一定不含Fe2O3 |

(1)步骤①样品用磁铁吸引前需经过研碎,其中研碎的目的是增大接触面积,使反应充分.
(2)步骤②中固体溶解时放出大量热,由此可以判断固体中一定含有CaO.写出该过程中的化学方程式CaO+H2O=Ca(OH)2.
(3)步骤③中反应的化学方程式是Na2CO3+Ca(OH)2=CaCO3↓+2NaOH.
北北同学对滤渣B又进行探究.
| 实验操作 | 实验现象 | 实验结论 |
| ①取滤渣B于试管中,加入适量稀盐酸 ②生成的气体通入澄清石灰水 | ①固体减少,有气泡冒出,溶液变为黄色②该溶液变浑浊. | 固体中一定含有CaCO3 和Fe2O3. |
 现有铜与金属镁、铁、锌中的一种组成的混合物,兴趣小组的同学欲测定其组成.进行以下实验,取该混合物粉末8.0g放入烧杯中,将140.0g 溶质的质量分数为14.0%的稀硫酸平均分四次加入该烧杯中,充分反应后,测得剩余固体质量数据记录如图.请你通过计算回答:
现有铜与金属镁、铁、锌中的一种组成的混合物,兴趣小组的同学欲测定其组成.进行以下实验,取该混合物粉末8.0g放入烧杯中,将140.0g 溶质的质量分数为14.0%的稀硫酸平均分四次加入该烧杯中,充分反应后,测得剩余固体质量数据记录如图.请你通过计算回答:
 小林同学在做探究质量守恒定律实验时,称取2.4g镁条在点燃的条件下与充足的空气反应,其反应的化学方程式为2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO,实验完毕后,称得所得固体的质量小于4.0g.
小林同学在做探究质量守恒定律实验时,称取2.4g镁条在点燃的条件下与充足的空气反应,其反应的化学方程式为2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO,实验完毕后,称得所得固体的质量小于4.0g.