题目内容
12.某化学兴趣小组的同学在分析某种含有三种溶质的无色溶液时,得出了以下结论.其中的三种溶质可能正确的是( )| A. | FeCl2、NaCl、Ba(OH)2 | B. | HCl、Na2CO3、AgNO3 | ||
| C. | Na2SO4、HCl、BaCl2 | D. | KCl、HCl、Al2(SO4)3 |
分析 本题利用复分解反应的条件来判断物质能否共存的问题,若物质在水中解离成的离子重新结合生成水或气体或沉淀时,物质就不能共存,本题还要注意能得到无色透明溶液,则应注意常见离子在水中的颜色.
解答 解:A、亚铁离子在溶液中显浅绿色,而该溶液是无色溶液,并且氯化亚铁可以和氢氧化钡反应生成氢氧化亚铁沉淀,这三种溶质不能在溶液中共存,故错误;
B、碳酸钠可以和盐酸、硝酸银之间相互反应,所以在溶液中不能共存,故错误;
C、氯化钡可以和硫酸钠反应生成硫酸钡沉淀,不能在溶液中共存,故错误;
D、三种溶质相互作用,不会生成沉淀、气体、水,所以在溶液中能够共存,且不存在带色的离子,故正确;
故选D.
点评 通过本题可以看出物质溶于水可能得到带颜色的溶液,在判断能否共存的同时还要注意习题的要求.

练习册系列答案
 夺冠训练单元期末冲刺100分系列答案
夺冠训练单元期末冲刺100分系列答案 新思维小冠军100分作业本系列答案
新思维小冠军100分作业本系列答案 名师指导一卷通系列答案
名师指导一卷通系列答案
相关题目
2.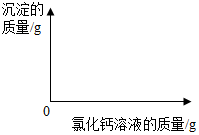 小明同学为了测定市面销售的某品牌纯碱(杂质为氯化钠)中碳酸钠的质量分数,进行了如下实验:
小明同学为了测定市面销售的某品牌纯碱(杂质为氯化钠)中碳酸钠的质量分数,进行了如下实验:
①在三个烧杯中分别加入11.0g样品;
②向三个烧杯中分别加入一定质量的10.0%氯化钙溶液;
③将充分反应后生成的沉淀过滤、洗涤、干燥,并称量得到的白色固体.
实验所得数据见下表,请你分析并进行有关计算:
(1)样品中碳酸钠的质量是多少?
(2)在图中绘制出白色沉淀与加入氯化钙溶液的质量关系图(图上要注明白色沉淀、氯化钙溶液的相关质量).
(3)充分反应后,烧杯Ⅱ中氯化钠的溶质质量分数是多少?
 小明同学为了测定市面销售的某品牌纯碱(杂质为氯化钠)中碳酸钠的质量分数,进行了如下实验:
小明同学为了测定市面销售的某品牌纯碱(杂质为氯化钠)中碳酸钠的质量分数,进行了如下实验:①在三个烧杯中分别加入11.0g样品;
②向三个烧杯中分别加入一定质量的10.0%氯化钙溶液;
③将充分反应后生成的沉淀过滤、洗涤、干燥,并称量得到的白色固体.
实验所得数据见下表,请你分析并进行有关计算:
| 烧杯Ⅰ | 烧杯Ⅱ | 烧杯Ⅲ | |
| 加入10.0%氯化钙溶液的质量(g) | 55.5 | 120.0 | 150.0 |
| 白色固体的质量(g) | 5.0 | 10.0 | 10.0 |
(2)在图中绘制出白色沉淀与加入氯化钙溶液的质量关系图(图上要注明白色沉淀、氯化钙溶液的相关质量).
(3)充分反应后,烧杯Ⅱ中氯化钠的溶质质量分数是多少?
7.下列诗词中没有涉及化学变化的是( )
| A. | 白玉为床金做马(《红楼梦》) | |
| B. | 春蚕到死丝方尽,蜡炬成灰泪始干(《无题》) | |
| C. | 爆竹声声一岁除,春风送暖人屠苏(《元日》) | |
| D. | 千锤万凿出深山,烈火焚烧若等闲(《石灰吟》) |
1.李铭同学想要探究甲、乙、丙三种物质溶解度的大小,于是他取来等质量的甲、乙、丙三种物质,并将它们分别放入三杯温度为t1℃的等质量的水中,用玻璃棒搅拌直至充分溶解,记录此时甲、乙、丙三种物质的剩余量情况,再将温度升温至t2℃,并再次记录下此时三种物质的剩余量情况,实验结束后李铭将记录的数据做成如表所示,下列说法中正确的是( )
| 物质 | 甲 | 乙 | 丙 |
| t1℃剩余质量(g) | 0 | 2 | 0.5 |
| t2℃剩余质量(g) | 2 | 0 | 3 |
| A. | t1℃时,甲物质的溶液一定是饱和溶液 | |
| B. | 甲物质的溶解度随温度的升高而增大 | |
| C. | t1℃和t2℃时,丙物质的溶液都为饱和溶液 | |
| D. | 乙物质的溶解度大于丙物质的溶解度 |
2.下列物质中既能跟稀H2SO4反应,又能跟氢氧化钠溶液反应的是( )
| A. | NaHCO3 | B. | Al2O3 | C. | Al(OH)3 | D. | Al |
 2015年化学实验操作考试中,有同学在做铁与硫酸铜溶液反应实验时,意外发现铁丝的表面有少量无色无味的气体产生,事后他们对该现象产生浓厚兴趣,想探究该气体的成分.
2015年化学实验操作考试中,有同学在做铁与硫酸铜溶液反应实验时,意外发现铁丝的表面有少量无色无味的气体产生,事后他们对该现象产生浓厚兴趣,想探究该气体的成分. 如图是以稀盐酸为例的反应关系体现了酸的化学性质,其中X与图中所给物质的类别不同,结合此图回答下列问题:
如图是以稀盐酸为例的反应关系体现了酸的化学性质,其中X与图中所给物质的类别不同,结合此图回答下列问题: