题目内容
19.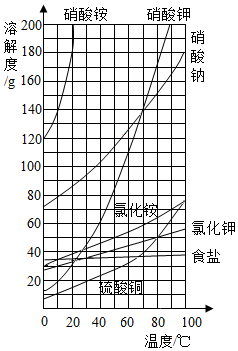 如图为几种固体的溶解度曲线,回答下列问题:
如图为几种固体的溶解度曲线,回答下列问题:(1)CuSO4的溶解度约为20g时,其对应的温度是20℃;若想使该饱和溶液转化为不饱和溶液,可采取的方法是升高温度(写出一种即可),用此方法后,溶液的质量分数没有(填“有”或“没有”)
发生变化.
(2)80℃时,140g NaNO3溶于100g水形成的溶液是不饱和溶液(填“饱和”或“不饱和”).
(3)20℃时,NH4NO3溶液的溶质质量分数最大为64.3%(计算结果保留到0.1%).
(4)若KNO3溶液中混有少量的NaCl杂质,可以采取降温结晶方法获得较纯净的KNO3固体.
(5)60℃时分别将等质量的KNO3、NaCl、CuSO4的饱和溶液各500g恒温蒸发掉100g水,析出晶体最多的是KNO3.
(6)60℃时,10g NaCl和90g KNO3完全溶解于100g蒸馏水中,冷却到30℃后,没有(“有”或“没有”)NaCl析出,有44.2g KNO3结晶析出.
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,根据溶解度的含义可以进行有关的分析与计算;②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)由CuSO4的溶解度曲线可以查出,CuSO4的溶解度约为20g时,其对应的温度是20℃;由于CuSO4的溶解度随温度的升高而增大,若想使该饱和溶液转化为不饱和溶液,可采取的方法是升高温度,用此方法后,溶液的质量分数没有发生变化.
(2)由NaNO3的溶解度曲线可以查出,在80℃时,NaNO3溶解度是150g,140g NaNO3溶于100g水形成的溶液是不饱和溶液.
(3)由NH4NO3的溶解度曲线可以查出,20℃时,NH4NO3溶解度是180g,饱和溶液的溶质质量分数最大,为:$\frac{180g}{180g+100g}×100%$≈64.3%.
(4)由溶解度曲线可知,由于KNO3的溶解度受温度的影响较大,NaCl的溶解度受温度的影响不大,若KNO3溶液中混有少量的NaCl杂质,可以采取降温结晶方法获得较纯净的KNO3固体.
(5)60℃时分别将等质量的KNO3、NaCl、CuSO4的饱和溶液各500g恒温蒸发掉100g水,由于KNO3的溶解度最大,析出晶体最多的是KNO3.
(6)由溶解度曲线可知,在30℃是氯化钠的溶解度是36.3g,KNO3的溶解度是45.8g,60℃时,10g NaCl和90g KNO3完全溶解于100g蒸馏水中,冷却到30℃后,没有NaCl析出,有 KNO3结晶析出,质量为:90g-45.8g=44.2g.
故答为:(1)20,升高温度,没有;(2)不饱和;(3)64.3%;(4)降温结晶;(5)KNO3;(6)没有,44.2g.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

| 选项 | 实验目的 | 实验方案 |
| A | 除去NaCl溶液中的Na2CO3 | 加适量稀硫酸 |
| B | 除去CaO中的CaCO3 | 加水溶解,过滤 |
| C | 除去CO2中的HCl气体 | 将混合气体通入NaOH溶液 |
| D | 除去KNO3溶液中的KCl | 加适量的AgNO3溶液,过滤 |
| A. | A | B. | B | C. | C | D. | D |
 2017年3月14日,113号元素被正式定名为“
2017年3月14日,113号元素被正式定名为“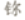 ”.鉨是研究人员用30号锌元素与83号铋元素碰撞发生核聚变的方法合成的.下列说法不正确的是( )
”.鉨是研究人员用30号锌元素与83号铋元素碰撞发生核聚变的方法合成的.下列说法不正确的是( )| A. |  的相对原子质量为286g 的相对原子质量为286g | B. |  的原子序数为113 的原子序数为113 | ||
| C. |  的核外电子数为113 的核外电子数为113 | D. | 锌和铋都属于金属元素 |
| A. | NH4NO3 | B. | K2CO3 | C. | KNO3 | D. | Ca(H2PO4)2 |
| A. | 硫在氧气中燃烧,火焰呈蓝紫色 | |
| B. | 在大理石上滴加稀盐酸,有气泡生成 | |
| C. | 氢氧化钠溶液中滴加硫酸铜溶液,生成蓝色絮状氢氧化铜沉淀 | |
| D. | 镁带在空气中燃烧,发出耀眼白光,生成白色固体 |
| A. | 甲、乙、丙、丁不可能含有同一种元素 | |
| B. | 若丙为盐、丁为水,则该反应一定为中和反应 | |
| C. | 甲、乙为化合物,则该反应一定为复分解反应 | |
| D. | 丙为CuCl2,则甲可能为氧化物、碱或盐 |
| A. | 空气中主要含氧气和氮气 | |
| B. | 拉瓦锡用定量的方法研究了空气的成分,得出氧气约占总质量的1/5 | |
| C. | 空气中的CO2是植物光合作用的重要原料 | |
| D. | 酸雨的产生与空气污染物SO2、NOx有关 |
| A. | 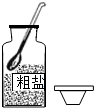 取用固体药品 | B. | 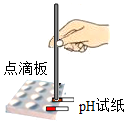 测溶液的pH 测溶液的pH | C. | 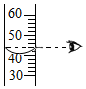 量取40mL溶液 | D. | 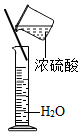 稀释浓硫酸 |
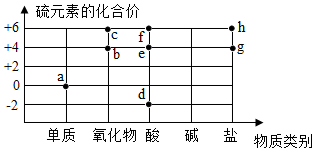 图中字母代表含硫元素的物质,下列判断错误的是( )
图中字母代表含硫元素的物质,下列判断错误的是( )| A. | 物质a在纯氧中燃烧可以生成物质b | B. | 物质c是二氧化硫 | ||
| C. | 物质d中硫元素的化合价为-2价 | D. | 物质d、e和f中一定都含有氢元素 |