题目内容
8.达菲是抗击甲型H7N9流感的有效药物,合成达菲的重要中间体为莽草酸(其化学式为:C7H10O5).下列有关莽草酸的说法不正确的是( )| A. | 莽草酸是一种有机化合物 | |
| B. | 莽草酸中C、H、O元素的质量比为7:10:5 | |
| C. | 莽草酸由三种元素组成 | |
| D. | 一个莽草酸分子中共有22个原子 |
分析 A、根据含有碳元素的化合物叫有机化合物,简称有机物,判断A的正确性;
B、根据物质中元素的质量比来分析;
C、根据化学式的意义判断是否正确;
D、根据化学式的意义判断B是否正确.
解答 解:A.莽草酸中含有C元素,是有机物;故正确;
B.莽草酸中C、H、O三种元素的质量比为:(12×7):(1×10):(16×5)=42:5:40;故错误;
C.莽草酸是由碳、氢、氧三种元素组成化合物,故正确;
D.该物质的一个分子中含有的原子数是:7+10+2=22,故正确.
故选B.
点评 解答此题只需根据化学式的含义及有关计算公式来分析计算过即可.

练习册系列答案
相关题目
19.某同学用被水润湿的pH试纸测得某液体的pH=5,则该液体pH的真实值( )
| A. | 等于5 | B. | 大于5 | C. | 小于5 | D. | 无法确定 |
16.某化学兴趣小组利用如图装置探究制取气体的原理、方法及性质.结合装置图,回答下列问题:
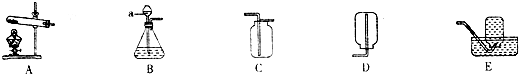
(1)写出图中标号仪器的名称:a长颈漏斗.
(2)用双氧水和二氧化锰制取氧气时,可选用的发生装置是B(填字母,下同),写出该反应的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,可选用C装置收集氧气,其原因是氧气的密度比空气的密度大,验证收集满的方法是将带火星的木条放在集气瓶口,若木条复燃,则证明收集满了;
(3)实验室常用氯化铵固体与碱石灰固体共热来制取氨气(NH3),应选择的发生装置是A.选择该装置的依据是反应物为固体,且需要加热;
(4)该化学兴趣小组同学通过加热15.5g氯酸钾和二氧化锰的混合物来制取氧气.测得反应时间与剩余固体的质量如表所示:
求:①T3时刻共产生氧气的质量是3.3g
②该小组取用的氯酸钾的质量是多少?

(1)写出图中标号仪器的名称:a长颈漏斗.
(2)用双氧水和二氧化锰制取氧气时,可选用的发生装置是B(填字母,下同),写出该反应的化学方程式:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,可选用C装置收集氧气,其原因是氧气的密度比空气的密度大,验证收集满的方法是将带火星的木条放在集气瓶口,若木条复燃,则证明收集满了;
(3)实验室常用氯化铵固体与碱石灰固体共热来制取氨气(NH3),应选择的发生装置是A.选择该装置的依据是反应物为固体,且需要加热;
(4)该化学兴趣小组同学通过加热15.5g氯酸钾和二氧化锰的混合物来制取氧气.测得反应时间与剩余固体的质量如表所示:
| 反应时间 | T0 | T1 | T2 | T3 | T4 | T5 | T6 |
| 剩余固体质量(g) | 15.5 | 15.5 | 14.2 | 12.2 | 11.1 | 10.7 | 10.7 |
②该小组取用的氯酸钾的质量是多少?
13.小明在实验操作技能考试中抽中的题目是:用固体氢氧化钠配制100g溶质质量分数为2%的NaOH溶液.他的有关做法正确的是( )
| A. | 选择的玻璃仪器有烧杯、托盘天平、量筒、玻璃棒、胶头滴管、试剂瓶 | |
| B. | 将NaOH固体放到滤纸上,用托盘天平称取2.0gNaOH | |
| C. | 用100mL量筒量取98.0mL水 | |
| D. | 用pH试纸测得2%的NaOH溶液的pH=13.6 |
20.比较、推理是化学学习常用的方法.如表是根据一些反应事实推导出的影响化学反应的因素,其中不合理的是( )
| 选项 | 化学反应事实 | 影响反应的因素 |
| A | H2O2遇二氧化锰后迅速分解,水遇二氧化锰不分解 | 催化剂 |
| B | 二氧化碳能与水反应生成碳酸,还能参与植物的光合作用,(二氧化碳和水在光照条件下反应生成葡萄糖和氧气) | 反应的条件 |
| C | 碳在常温下不与氧气反应,在点燃时能与氧气反应 | 反应的温度 |
| D | 红热的铁丝在空气中很难燃烧,在氧气中能剧烈燃烧 | 反应物的浓度 |
| A. | A | B. | B | C. | C | D. | D |
17.市售加碘盐是在食益中加入一定量的碘酸钾(KIO3),KIO3中碘元素的化合价是( )
| A. | +5 | B. | -1 | C. | +3 | D. | +1 |
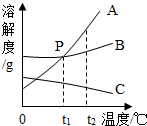 如图是A、B、C三种固体物质的溶解度曲线,请回答:
如图是A、B、C三种固体物质的溶解度曲线,请回答: