题目内容
18.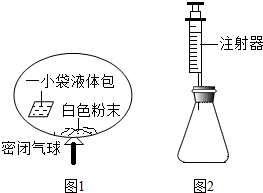 某研究小组对自动充气气球(示意图如图1)进行下列探究.
某研究小组对自动充气气球(示意图如图1)进行下列探究.[查阅资料]该气球充气原理是:通过挤破液体包,使液体与白色粉末接触产生二氧化碳气体,实现气球自动充气.
(1)为检验气体是二氧化碳,可选用氢氧化钙溶液(填试剂名称).
探究一:液体包内溶液酸碱性的探究
(2)室温时,用pH试纸测得溶液的pH=3,则该溶液呈酸性.
探究二:白色粉末成分的探究
[猜想与假设]甲同学认为是碳酸钙;乙同学认为是碳酸钠;丙同学认为是碳酸氢钠.
[设计并进行实验]
(3)将少量白色粉末放入水中搅拌,固体全部溶解,说明甲同学的猜想不正确(填“正确”或“不正确”).
(4)室温时,分别向盛有碳酸氢钠、碳酸钠和白色粉末样品的锥形瓶中注入等体积、足量的10%盐酸(装置如图2),记录如表:
| 实验编号 | 锥形瓶内物质 | 最终得到CO2体积/mL | |
| 名称 | 质量/g | ||
| ① | 碳酸氢钠 | 0.10 | V1 |
| ② | 碳酸钠 | 0.10 | V2 |
| ③ | 白色粉末 | a | V1 |
[分析并得出结论]
(5)如何从上表中获取证据并得出结论?根据实验1.3可知,最终得到的二氧化碳体积相等,因此,白色粉末是碳酸氢钠.
分析 (1)根据二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水进行分析;
(2)根据pH小于7的溶液显酸性进行分析;
(3)根据碳酸钙难溶于水进行分析;
(4)根据碳酸氢钠和盐酸反应生成氯化钠、水和二氧化碳,控制变量法的正确操作方法进行分析;
(5)根据表中的数据进行分析.
解答 解:(1)二氧化碳和氢氧化钙反应生成碳酸钙沉淀和水,所以为检验气体是二氧化碳,可选用氢氧化钙溶液;
(2)pH小于7的溶液显酸性,所以室温时,用pH试纸测得溶液的pH=3的溶液呈酸性;
(3)碳酸钙难溶于水,所以将少量白色粉末放入水中搅拌,固体全部溶解,说明甲同学的猜想不正确;
(4)碳酸氢钠和盐酸反应生成氯化钠、水和二氧化碳,化学方程式为:NaHCO3+HCl=NaCl+H2O+CO2↑,碳酸氢钠、碳酸钠的质量都是0.1g,为了形成对比,所以a的质量也是0.1g,每84份质量的碳酸氢钠会生成44份质量的二氧化碳,每106份质量的碳酸钠会生成44份质量的二氧化碳,所以V1>V2;
(5)根据实验1.3可知,最终得到的二氧化碳体积相等,因此,白色粉末是碳酸氢钠.
故答案为:(1)氢氧化钙溶液;
(2)酸;
(3)不正确;
(4)NaHCO3+HCl=NaCl+H2O+CO2↑,0.1,>;
(5)根据实验1.3可知,最终得到的二氧化碳体积相等,因此,白色粉末是碳酸氢钠.
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.

练习册系列答案
相关题目
8.下列实际应用中,与中和反应原理无关的是( )
| A. | 用氢氧化钠溶液洗涤石油产品中的残余硫酸 | |
| B. | 用酸洗去金属表面的铁锈 | |
| C. | 用熟石灰改良酸性土壤 | |
| D. | 用稀氨水涂抹在蚊子叮咬处(蚊子能分泌出蚁酸)止痒 |
9. 2014年科学家用钙(Ca)原子轰击锫(Bk)原子,确定合成了117号元素,填补了元素周期表最后一个空格,如图.下列说法错误的是( )
2014年科学家用钙(Ca)原子轰击锫(Bk)原子,确定合成了117号元素,填补了元素周期表最后一个空格,如图.下列说法错误的是( )
 2014年科学家用钙(Ca)原子轰击锫(Bk)原子,确定合成了117号元素,填补了元素周期表最后一个空格,如图.下列说法错误的是( )
2014年科学家用钙(Ca)原子轰击锫(Bk)原子,确定合成了117号元素,填补了元素周期表最后一个空格,如图.下列说法错误的是( )| A. | 该元素原子的核外电子数为117 | B. | 该元素的原子序数为117 | ||
| C. | 该元素原子的中子为117 | D. | 钙和锫都属于金属元素 |
6.2016年4月22日世界地球日主题是“节约集约利用资源,倡导绿色简约生活”,下列活动不符合该主题的是( )
| A. | 使用乙醇汽油能减少污染,节约石油资源 | |
| B. | 开展“节约一滴水从我做起”等活动 | |
| C. | 防治植物秸秆污染土壤,将秸秆就地焚烧 | |
| D. | 收集丢弃的塑料瓶、易拉罐、废报纸等变废为宝 |
3.治污水是“五水共治”内容之一,根据国家标准,废水排放时铅元素的含量不允许超过1.0毫升/升,蓄电池生产企业往往采用化学沉淀法处理Pb2-,其中以氢氧化物沉淀法应用较多.
(1)根据图表信息,沉淀剂除了NaOH外,还可使用的两种钠盐是碳酸钠和硫化钠.
20℃时,各种铅的化合物在水中的溶解度
(2)在弱碱性环境中,氢氧化铅的沉淀更完全,此时废水经沉淀过滤后,检测出铅元素含量仅为0.0207毫克/升,假设废水中的铅元素全部以Pb(OH)2形式存在,请你通过计算确定,此时1升废水中溶解的Pb(OH)2是多少毫克?
(3)某蓄电池生产企业购得40%的烧碱溶液100千克,若废水处理时需要溶质质量分数为10%的NaOH溶液,则应对所购烧碱溶液加水300千克进行稀释.
(1)根据图表信息,沉淀剂除了NaOH外,还可使用的两种钠盐是碳酸钠和硫化钠.
20℃时,各种铅的化合物在水中的溶解度
| 物质 | 溶解度/g | 物质 | 溶解度/g |
| Pb(NO3)2 | 54.3 | PbCO3 | 7.3×10-3 |
| Pb(OH)2 | 1.6×10-4 | PbS | 6.8×10×10-13 |
(3)某蓄电池生产企业购得40%的烧碱溶液100千克,若废水处理时需要溶质质量分数为10%的NaOH溶液,则应对所购烧碱溶液加水300千克进行稀释.
10.分类法是化学学习的重要方法之一,下列各组物质按照单质、盐、混合物的顺序排列的是( )
| A. | 生铁、氢氧化铜、冰水混合物 | B. | 液氧、硫酸钡、粗盐 | ||
| C. | 天然气、纯碱、石油 | D. | 钙片、氯化镁、海水 |
20.在水溶液中可以大量共存的一组离子是( )
| A. | H+、K+、OH- | B. | Na+、H+、HCO3- | C. | Fe3+、NO3-、OH- | D. | H+、NH4+、Cl- |
 根据给出的元素周期表中部分原子的结构示意图,回答问题.
根据给出的元素周期表中部分原子的结构示意图,回答问题. ,推测氧元素在元素周期表中应排在第二周期.
,推测氧元素在元素周期表中应排在第二周期.