题目内容
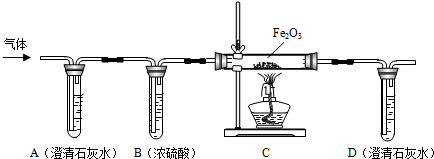
9.现在的人们对大气环境越来越重视,环保局对大气质量也有一定的标准,SO2是大气主要污染物之一,某中学研究性学习小组到炼铜厂附近测定周围环境中SO2的含量,他们设计了如图所示的装置进行实验,并根据环保标准来判断污染等级.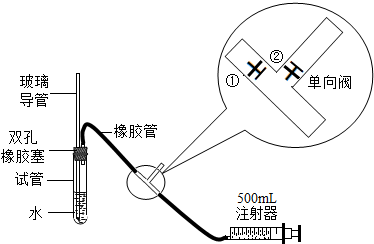
我国环境空气质量标准中对每次空气质量测定中的SO2最高质量分数限值
| SO2最高质量分数限值(单位:mg/m3) | ||
| 一级标准 | 二级标准 | 三级标准 |
| 0.15 | 0.50 | 0.70 |
②二氧化硫与碘水的反应为:SO2+I2+2H2O═H2SO4+2HI,向试管中加入2.0mL溶质质量分数为0.0127%的碘水(此时溶液的密度与水的密度相近),用适量的蒸馏水稀释后再加入2~3滴淀粉溶液A.测定指定地点的空气中SO2含量时,推拉注射器的活塞反复抽气,A溶液由蓝色变为无色时反应恰好完全进行.
(注:单向阀原理说明:当注射器推活塞时,①关闭,②打开;当注射器拉活塞时,①打开,②关闭.)
(3)研究性学习小组使用如上实验装置和溶液A,测量某地空气中的SO2含量(所用装置和药品均无问题).当反应恰好完全进行,记录抽气次数为240次(假设每次抽气500mL).请计算该地空气中SO2的质量分数并判断该地SO2含量的标准.
分析 弄清装置气密性的检验必须要保证装置能形成一个密闭的体系和引起密闭体系内的压强的变化,由于当注射器推活塞时,①关闭,②打开;当注射器拉活塞时,①打开,②关闭,因此检查该装置的气密性时,为使形成一个密闭的空间,应拉注射器的活塞,使装置内的压强减小,从而在浸没在水中的玻璃导管口会看到有气泡冒出.由于SO2+I2+2H2O=H2SO4+2HI,当单质碘恰好完全反应时,淀粉遇碘变成的蓝色就会消失,从而根据参加反应的碘的质量即可求出二氧化硫的质量,从而确定此地空气中二氧化硫的含量.
解答 解:①弄清装置气密性的检查必须要保证装置形成一个密闭的体系和引起体系内压强变化,由于当注射器推活塞时,①关闭,②打开;当注射器拉活塞时,①打开,②关闭,因此检查该装置气密性时,为使装置形成一个密闭的空间,应拉注射器的活塞,使装置内压强减小,从而在浸没水中的玻璃管口会看到气泡冒出;故填:浸没在水中的玻璃导管口有气泡冒出;
②由于SO2+I2+2H2O=H2SO4+2HI,当碘单质恰好反应,淀粉遇到碘变成的蓝色就会消失;故填:蓝.
(3)设恰好完全反应时,二氧化硫的质量为x,
SO2+I2+2H2O═H2SO4+2HI,
64 254
x 2mL×1g/mL×0.00127%
$\frac{254}{2mL×1g/mL×0.00127%}$=$\frac{64}{x}$,
x=0.0000064g=0.0064mg,
240次抽取的气体体积为:500mL×240=120000mL=0.12m3,
二氧化硫的含量为:0.0064mg/0.12m3=0.053mg/m3<0.15mg/m3;
所以属于一级标准.
故填:0.053mg/m3;一级标准.
点评 本题考查了物质组成实验测定方法和过程分析判断,主要是 二氧化硫气体体积的测定试验方法的理解应用,掌握基础是关键,题目难度中等.

| A. | 14.6g | B. | 3.6g | C. | 3.2g | D. | 1.4g |
| A. | 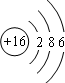 | B. | 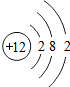 | C. | 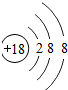 | D. | 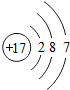 |
 ”表示氢原子,下列方框中能表示2H2的意义的是( )
”表示氢原子,下列方框中能表示2H2的意义的是( )| A. |  | B. | 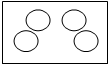 | C. | 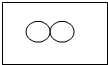 | D. | 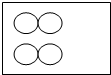 |
| A. | 甲和乙是同一种原子 | B. | 甲和乙是同一种元素 | ||
| C. | 乙和丙的核电荷数相等 | D. | 乙和丙互为同位素原子 |
| A. | 倒出仍是饱和食盐水 | B. | 倒出溶液的溶质质量分数变小了 | ||
| C. | 倒出溶液的溶解度变小 | D. | 倒出溶液的溶质质量分数变大了 |