题目内容
3.某无色溶液,在pH=0和pH=14的条件下都能大量共存的是( )| A. | Fe2+、K+、SO42-、NO3- | B. | Mg2+、NH4+、SO42-、Cl- | ||
| C. | Na+、K+、CO32-、MnO4- | D. | Ba2+、Na+、NO3-、Cl- |
分析 pH为0的水溶液显酸性,水溶液中含有大量的H+;pH为14的水溶液显碱性,水溶液中含有大量的OH-;根据复分解反应发生的条件可知,若物质之间相互交换成分不能生成水、气体、沉淀,则能够在溶液中大量共存.
解答 解:pH为0的水溶液显酸性,水溶液中含有大量的H+;pH为14的水溶液显碱性,水溶液中含有大量的OH-.
A、Fe2+和碱性溶液中的氢氧根离子能能结合生成氢氧化亚铁沉淀,不能在pH=14的条件下大量共存,故选项错误.
B、NH4+和碱性溶液中的氢氧根离子能能结合生成氨气和水,Mg2+和碱性溶液中的氢氧根离子能能结合生成氢氧化镁沉淀,不能在pH=14的条件下大量共存,故选项错误.
C、CO32-与酸性溶液中的氢离子能能结合生成水和二氧化碳,不能在pH=0的条件下大量共存;故选项错误.
D、四种离子在溶液中相互交换成分不能生成沉淀、气体、水,能在酸性溶液和碱性溶液中大量共存,故选项正确.
故选:D.
点评 本题考查了离子共存的问题,判断各离子在溶液中能否共存,主要看溶液中的各离子之间能否发生反应生成沉淀、气体、水;还要注意是在酸性或碱性溶液中共存.

练习册系列答案
相关题目
3.在托盘天平的两个托盘上各放一只烧杯,两只烧杯中都盛有过量的相同质量分数的盐酸,天平两边保持平衡,此时向左边烧杯中加入5.6gCaO,若使天平两边再次保持平衡,需向右边烧杯中加入CaCO3的质量为( )
| A. | 5.6g | B. | 17.6g | C. | 10g | D. | 11.2g |
14.下列实验操作中,正确的是( )
| A. | 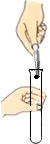 取块状固体 | B. |  闻气体气味 | C. | 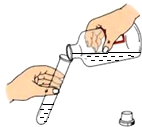 倾倒液体 | D. | 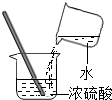 稀释浓硫酸 稀释浓硫酸 |
11.将鸡蛋壳浸入稀盐酸中,有气泡产生,这是因为鸡蛋壳中含有( )
| A. | 硫酸根 | B. | 氢氧根 | C. | 碳酸根 | D. | 硝酸根 |
18.通过下列各组对比实验,能得到相应结论的是( )
| 实验方案 | 实验结论 | ||
| 实验? | 实验? | ||
| A | 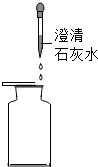 空气 | 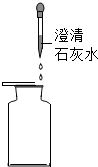 人呼出的气体 | 人呼出的气体全部是CO2 |
| B | 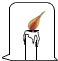 | 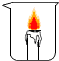 | 燃烧需要可燃物的温度达到着火点 |
| C | 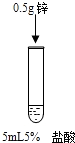 | 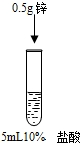 | 盐酸的浓度对反应剧烈程度有影响 |
| D | 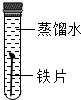 | 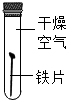 | 铁生锈需要氧气和水 |
| A. | A | B. | B | C. | C | D. | D |
8.将下列试剂分别滴入硝酸铜溶液,碳酸钠溶液和稀盐酸中,能观察到三种不同现象的是( )
| A. | 氢氧化钾溶液 | B. | 氯化钡溶液 | C. | 氢氧化钙溶液 | D. | 氯化钾溶液 |